Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Проблема антибиотикорезистентности
Helicobacter pylori у детей и выбор терапии
Е.А. Корниенко, Н.И. Паролова
Причиной недостаточной эффективности терапии многих
гастродуоденальных заболеваний является возрастающая
резистентность к антибиотикам Helicobacter pylori (Н.pylori),
что обусловлено мутациями различных генов. Наибольшее
практическое значение имеют мутации 23S rРНК, лежащие в
основе резистентности к кларитромицину. Согласно
международному консенсусу Маастрихт-3, схема с ингибитором
протонной помпы (ИПП), кларитромицином и метронидазолом
рекомендована в качестве терапии 1 линии. Целью работы
была оценка резистентности Н.pylori к кларитромицину с
помощью ПЦР-диагностики мутации 23S rРНК в биоптате
слизистой оболочки желудка и оценка эффективности
стандартной схемы в сравнении со схемами с одним
антибиотиком - амоксициллином, Де-нолом и ИПП. Обследовано
68 детей с Н.pylori - ассоциированными заболеваниями,
резистентность Н.pylori к кларитромицину составила 28%.
Эффективность стандартной схемы продолжительностью 10 дней
составила 14%. Эффективность схемы с амоксициллином,
Де-нолом и омепразолом продолжительностью 7 дней составила
40%, продолжительностью 10 дней - 75%, при замене
омепразола на эзомепразол эффективность составила 83%.
Схема с одним антибиотиком отличалась хорошей
переносимостью.
Ключевые слова: Helicobacter pylori,
антибиотикорезистентность, эрадикация.
Открытие H.pylori и доказательство его ведущей роли в
развитии большинства гастродуоденальных заболеваний
кардинальным образом изменило подход к их лечению.
Хронический гастрит, язвенная болезнь, лимфома желудка,
ассоциированные с Н.pylori-инфекцией, требуют проведения
терапии, направленной на уничтожение микроба. В последние
годы отмечено нарастание неудач при проведении 7-дневных
тройных схем эрадикационной терапии [1,2,3]. Главной
причиной их является антибиотикорезистентность Н.pylori.
Развитие резистентности Н.pylori к антибиотикам связано с
точечными мутациями различных генов (табл.1)
ТАБЛИЦА 1. Генетические мутации
как причины антибиотикорезистентности Helicobacter pylori
| Антибиотики |
Мутирующие гены
|
Макролиды
Метронидазол
Фторхинолоны
Рифампицин
Амоксициллин
Тетрациклин |
23S РНК
rdxA, frxA
gyrA
rpoB
pbp-1A
16S РНК
|
Так, резистентность к кларитромицину связана с изменением
конфигурации рибосом вследствие точечной мутации в домене
V 23S rРНК [4]. Причина резистентности к метронидазолу до
сих пор окончательно не установлена. Очевидно, наиболее
важна альтерация rdxA-гена, но может быть вовлечение
frxA-гена [5,6]. Низкая чувствительность к амоксициллину
возможна вследствие мутаций pbp1-гена, определяющего
способность белков Н.pylori связывать пенициллины [7]. К
счастью, последняя наблюдается крайне редко, поэтому
микроб сохраняет почти 100% чувствительность к
амоксициллину. Плазмидная передача устойчивости лактамазы
также не свойственна Н.pylori.
В 1999-2002г в Европе было проведено проспективное
мультицентровое исследование, включавшее 16 педиатрических
центров в 14 странах [8]. Всего было обследовано 1233
пациента, 41% которых были родом из Африки и Ближнего
Востока. Исследовалась как первичная (до лечения), так и
вторичная (при неудачном лечении) резистентность.
Первичная резистентность к кларитромицину была выявлена у
20% детей, вторичная – у 42%. Первичная резистентность к
кларитромицину была достоверно выше у детей до 6 лет, чем
у подростков старше 12 лет и преобладала у жителей Южной
Европы по сравнению с Северной. Эти различия легко
объяснимы более частым назначением макролидов для лечения
внежелудочных (в основном, респираторных) заболеваний у
детей раннего возраста и существованием определенных
ограничений в назначении препаратов этой группы в
северо-европейских странах. В Восточной Европе отдельные
исследования также показали высокую резистентность к
кларитромицину у детей. Так, в Болгарии она составила
12,4%, а в Польше - 23,5% [9]. В России подобное
исследование было проведено в 2000г Л.В. Кудрявцевой,
резистентность к кларитромицину у взрослых в Москве
составила 13% [10]. Рядом исследований была показана
тенденция к росту резистентности к кларитромицину: так, в
США и Канаде до 2000 г. она составляла 4%, а в 2004г -
11-12% [11].
Основной причиной роста резистентности Н.pylori к
кларитромицину является не столько предшествующая
неэффективная эрадикационная терапия, сколько широкое
использование макролидов при лечении других заболеваний.
Поскольку дети чаще получают препараты этой группы, то и
распространенность устойчивых штаммов Н.pylori среди них
существенно выше, чем у взрослых. Так, исследование,
проведенное в японских семьях, показало, что хотя члены
одной семьи обычно заражены идентичными штаммами Н.pylori,
резистентность к кларитромицину выше у детей [12]. В
целом, резистентность Н.pylori к кларитромицину возрастает
пропорционально его потреблению в данном регионе [13]. Все
препараты группы макролидов характеризуются развитием
перекрестной резистентности штаммов in vitro, но не все
макролиды в равной мере могут формировать таковую у
Н.pylori in vivo, поскольку это зависит также от
способности препарата накапливаться в слизистом слое.
Поскольку кларитромицин быстро достигает ингибирующей
концентрации на поверхности слизистой оболочки желудка,
после курса лечения 2/3 не уничтоженных штаммов Н.pylori
становятся резистентными к нему. Этого нельзя сказать об
азитромицине - он имеет низкую эффективность эрадикации
(62%), но вторичная резистентность развивается только в
23% случаев [14].
Резистентность Н.pylori к метронидазолу варьирует от 20 до
40% в Европе и США, но она значительно выше в
развивающихся странах (50-80%) [9]. За последнюю декаду ХХ
века в Европе произошло небольшое нарастание
резистентности к метронидазолу: в 1991г она составляла в
среднем 27, 5% [15], а в 2000г - 33,1% [13]. В России
резистентность к метронидазолу выше, в 2001г в Москве и
Петербурге она составила 55% [10], но в последние годы
имеет тенденцию к снижению (42%).
Интересно отметить, что частота антибиотикорезистентных
штаммов Н.pylori выше у больных хроническим гастритом
(16,7% к кларитромицину, 56,4% к метронидазолу), чем
язвенной болезнью (5,6% к кларитромицину, 19,8% к
метронидазолу) [16]. Возможно, это связано с более высоким
уровнем потребления антибиотиков у больных хроническим
гастритом в целом, но не исключено также и влияние
особенностей токсигенности штаммов Н.pylori. Так, при
язвенной болезни почти все штаммы CagA-позитивны, в то
время как при хроническом гастрите только две трети [17].
Как известно, токсигенные штаммы характеризуются более
плотной адгезией к желудочному эпителию, что, возможно,
улучшает условия воздействия на них антибиотиков, повышает
эффективность терапии и снижает необходимость назначения
повторных курсов лечения. Нами также было показано ранее,
что более низкий процент эрадикации может объясняться
иммунологической недостаточностью у пациентов с нодулярным
гастритом и у детей в возрасте до 7 лет [17].
Необходимо подчеркнуть несоответствие результатов разных
методов оценки резистентности Н.pylori к метронидазолу.
Если в определении резистентности к кларитромицину
достоверность диагностики мутации 23S РНК с помощью ПЦР
или флюоресцентной гибридизации in situ не вызывает
сомнений, то методы обнаружения резистентности к
метронидазолу основаны на бактериологической диагностике
(метод дисков, Е-тест) и до сих пор не стандартизованы.
Возможно, этим объясняется нередкое несовпадение
результатов, полученных in vitro, и эффективности терапии
in vivo.
Тем не менее, даже с учетом возможных погрешностей в
определении резистентности Н.pylori к метронидазолу, можно
делать вывод о высоком, среднем или низком в целом ее
уровне в популяции. Российские данные указывают на
довольно высокую резистентность Н.pylori к метронидазолу
[10]. Антибиотикорезистентность Н.pylori является главной
причиной неэффективности терапии. Так, суммируя результаты
20 европейских исследований, в которых проведена оценка
результатов стандартной тройной терапии 1 линии,
включавшей ИПП, амоксициллин и кларитромицин у 2751
пациента, можно заключить, что в случае чувствительности
штаммов эрадикация достигается в среднем у 87,8%, а при
устойчивости к кларитромицину - только у 18,3% пациентов
[9]. Это 70% снижение эффективности лечения подчеркивает
клиническое значение резистентности Н.pylori к
кларитромицину. Еще более интересны результаты тройной
терапии, включавшей ИПП, метронидазол и кларитромицин. В
случае чувствительности Н.pylori к обоим антибиотикам
эрадикация достигалась у 97%, при резистентности к
кларитромицину - у 50%, к метронидазолу - у 72,6%, к обоим
антибиотикам - ни у одного пациента. То есть, устойчивость
к кларитромицину приводит в любом сочетании к
существенному снижению эффективности терапии. В то же
время, устойчивость к метронидазолу в меньшей степени
отражается на результатах лечения, особенно при удлинении
курса лечения до 10-14 дней [18]. На основании этих данных
сочетание кларитромицина и метронидазола было признано
более эффективным, чем амоксициллина и кларитромицина на 1
линии терапии, а продолжительность лечения было
рекомендовано удлинить до 14 дней. Это легло в основу
рекомендаций Маастрихт-3-2005, однако такое сочетание
применимо лишь в популяциях с высокой чувствительностью к
обоим антибиотикам. В случае резистентности к
метронидазолу выше 40% и кларитромицину выше 15-20%
применение этих антибиотиков нецелесообразно [20]. Целью
данной работы явилась оценка резистентности к
кларитромицину у детей с Н.pylori-ассоциированными
заболеваниями и разработка схем эрадикации Н.pylori,
приемлемых для популяции с высокой
антибиотикорезистентностью.
Материал и методы:
Под нашим наблюдением находились 68 пациентов в
возрасте от 10 до 17 лет с хроническими заболеваниями
верхних отделов пищеварительного тракта, ассоциированных с
инфекцией Н.pylori: язвенная болезнь двенадцатиперстной
кишки (ЯБДПК) была диагностирована у 16 человек,
хронический гастродуоденит (ХГ) - у 42 человек. В
исследование были включены лишь дети, не получавшие ранее
антихеликобактерной терапии. Пациенты, получавшие в
течение последних 3 месяцев антибактериальную терапию по
поводу других заболеваний, в исследование не включались.
С целью определения чувствительности Н.pylori к
кларитромицину использовали ПЦР в биоптате слизистой
оболочки антрального отдела желудка для выявления точечной
мутации 23S РНК, исследование проводилось в лаборатории
молекулярной генетики больницы №31 г. Санкт-Петербурга.
В соответствии с выбранной схемой терапии, дети были
разбиты на 4 группы, идентичные по возрасту, полу и
характеру гастродуоденальной патологии. В 1 группу вошли
дети, получавшие схему, рекомендованную консенсусом
Маастрихт-3. Пациенты остальных групп получали схемы с
одним антибиотиком - амоксициллином, к которому не
отмечено резистентности Н.pylori, но при этом схемы в
группах отличались по продолжительности (7 дней во 2
группе, в остальных 10 дней) или по типу ИПП (эзомепразол
или омепразол).
Группа 1: (25 пациентов)
- Эзомепразол (Нексиум) 40 мг 2раза в день,
- Кларитромицин 0,5 г 2 раза в день,
- Метронидазол 0,5 г 2 раза в день,
- Продолжительность - 10 дней.
Группа 2: (10 пациентов)
- Омепразол (Хелол) 20 мг 2 раза в день,
- Де-нол 120 мг 4 раза в день,
- Амоксициллин (Флемоксин-солютаб) 1,0 г 2 раза в
день,
- Продолжительность - 7 дней.
Группа 3: (23 пациента)
- Омепразол (Хелол) 20 мг 2 р в день,
- Де-нол 120 мг 4 раза в день,
- Амоксициллин (Флемоксин-солютаб) 1,0 г 2 раза в
день,
- Продолжительность - 10 дней/
Группа 4: (10 пациентов)
- Эзомепразол (Нексиум) 40 мг 2 р в день,
- Де-нол 120 мг 4 раза в день,
- Амоксициллин (Флемоксин-солютаб) 1,0 г 2 раза в
день,
- Продолжительность - 10 дней.
Для установления диагноза мы использовали стандартные
методы обследования: ФЭГДС с биопсией из тела и
антрального отдела желудка, гистологическое исследование
биоптатов. Для диагностики Н.pylori, наряду с
гистологическим исследованием, применяли быстрый уреазный
тест (Хелпил-тест®), дыхательный Хелик-тест® ООО «АМА».
Обследование с использованием всех вышеперечисленных
методов проводилось до начала терапии и спустя 6 недель
после завершения лечения.
Для оценки антисекреторной эффективности ингибиторов
протонной помпы (ИПП) проводилась суточная рН-метрия с
помощью аппарата "Гастроскан-24" на пятый день терапии.
Для оценки переносимости схемы использовались анкеты с
ежедневным внесением данных об объективных и субъективных
симптомах у каждого пациента.
Результаты:
При определении чувствительности Н.pylori к
кларитромицину из 68 обследованных пациентов точечные
мутации 23S РНК обнаружены у 19 детей, что составило 28%.
Данные суточного мониторинга рН, проведенного на 5 день
приема ИПП показали, что средний рН в теле желудка на фоне
приема омепразола составил 4,88, а на фоне приема
эзомепразола - 5,9.
Анализ субъективных и объективных симптомов показал, что
стандартной схема, рекомендованная Маастрихт-3 (ИПП+кларитромицин+метронидазол),
в 60% сопровождалась побочными реакциями в виде усиления
болей в животе (17%), диареи (7%), тошноты (23,5%) и рвоты
(12%). Схема с одним антибиотиком, независимо от
продолжительности (7 или 10 дней) и выбора ИПП (омепразол
или эзомепразол), хорошо переносилась детьми и лишь в
10-11% сопровождалась небольшой тошнотой. Болевой синдром
был купирован несколько быстрее у пациентов 2-4 групп (в
среднем на 3 день), чем в 1 группе (на 4-5 день).
Контрольное исследование через 6 недель показало, что
среди детей 1 группы, получавших стандартную схему (ЭКМ),
эрадикация была достигнута лишь в 14%. Пациенты 2 группы,
получавшие схему с одним антибиотиком (ОДА) в течение 7
дней, имели более высокий, но также недостаточный
показатель эрадикации - 40%. При удлинении этой схемы до
10 дней (3 группа) эрадикация достигалась уже в 75%.
Замена омепразола на эзомепразол в этой схеме (4 группа)
позволило увеличить эффективность лечения и достичь
эрадикации в 83%. (рис. 1).
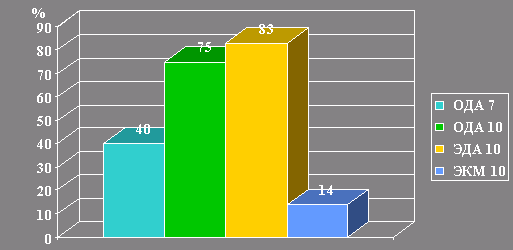
Рис. 1. Эффективность схем
эрадикации:
ОДА7 – омепразол+Де-нол+амоксициллин 7 дней,
ОДА10 – омепразол+Де-нол+амоксициллин 10 дней,
ЭДА 10 – эзомепразол+Де-нол+амоксициллин 10 дней,
ЭКМ 10 – эзомепразол+кларитромицин+метронидазол 10 дней.
Обсуждение:
Эрадикация Н.pylori является основой лечения
наиболее тяжелых форм гастродуоденальной патологии у
детей. Долгосрочные катамнестические наблюдения
подтверждают уменьшение частоты обострений язвенной
болезни, возможность обратного развития начальных
атрофических изменений после успешной эрадикации Н.pylori
[17, 21]. Своевременная антихеликобактерная терапия,
проведенная в детском возрасте, может уменьшить риск
развития рака желудка и вероятность некоторых
внежелудочных, в частности, аутоиммунных, заболеваний в
дальнейшем [22]. Вместе с тем, неудовлетворительные
практические результаты классических эрадикационных схем,
высокий уровень антибиотикорезистентности Н.pylori в
России заставляют проводить повторные курсы лечения, делая
терапию еще более агрессивной и усиливая скептицизм
врачей. В соответствии с Международными рекомендациями
Маастрихт-3-2005, оптимальной схемой 1 линии может быть
схема, включающая ИПП, кларитромицин и метронидазол
продолжительностью 14 дней. Однако эта схема может быть
назначена только при условии популяционной резистентности
в регионе, не превышающей 40% к метронидазолу и 20% к
кларитромицину. В России резистентность Н.pylori к
метронидазолу достигла критического порога (42%).
Резистентность к кларитромицину была до недавнего времени
изучена только у взрослых, у них она казалась допустимой -
13%. Наше исследование, хотя и ограниченное по
численности, показало значительно более высокий показатель
резистентности у детей – 28%, что превышает допустимый
порог. То есть, рекомендуемая Маастрихтом-3 терапия 1
линии в условиях России мало приемлема, и наше
исследование это подтвердило - эрадикация была достигнута
лишь у 14% больных. К тому же, схема с кларитромицином и
метронидазолом плохо переносится детьми, поэтому не может
быть рекомендована в детской отечественной практике. Среди
основных антибиотиков, используемых для терапии
Н.pylori-ассоциированных заболеваний, только амоксициллин
может не вызывать сомнений в чувствительности к нему
возбудителя. Как строить схему лечения в этих условиях?
Можно пойти по пути поиска новых и новых антибиотиков, но
это неизбежно будет увеличивать круг резистентности и
никак не снизит агрессивность лечения.
Мы выбрали другой путь, руководствуясь первой заповедью
Гиппократа: «Не вреди». Мы ограничились одним
антибиотиком, к которому сохраняется чувствительность
Н.pylori - амоксициллином, дополнив его наиболее
эффективным препаратом висмута - Де-нолом, обладающим
синергизмом с антибиотиками и одновременным
цитопротективным действием. Возможности этого препарата
действовать даже на кокковые и внутриклеточные формы
Н.pylori, отличные от антибиотиков точки приложения,
отсутствие резистентности к нему представлялись нам более
оптимальными, чем поиск новых сочетаний антибиотиков.
Эффективное подавление желудочной секреции также является
залогом успешной эрадикационной терапии. Многие
антибиотики разрушаются в кислой среде желудка, в
частности, амоксициллин действует только при рН выше 4.
Поэтому правильный выбор антисекреторного препарата может
повышать результативность лечения. Среди всех ИПП наиболее
изучен омепразол, в мире накоплен достаточно большой опыт
его использования в педиатрической практике, в том числе у
детей раннего возраста. Большинство клинических и
фармакокинетических исследований, проведенных у детей,
показало, что для достижения антисекреторного эффекта в
течение 24 часов оптимальна доза омепразола 1 мг/кг/сут.
Недавно появившийся левовращающий изомер омепразола
эзомепразол отличается более медленным выведением и, как
следствие, более продолжительным подавлением желудочной
секреции. Препарат широко апробирован у взрослых, при
изучении его фармакокинетики у детей было показано, что,
начиная с 3-хмесячного возраста, она не отличается от
таковой у взрослых. Поэтому эзомепразол, также как
омепразол, был официально рекомендован ESPGHAN для лечения
кислотозависимых заболеваний у детей старше 3 мес., при
этом его эквивалентная доза в два раза выше, чем доза
омепразола. Проведенная нами оценка антисекреторного
действия омепразола и эзомепразола в эквивалентных дозах
показала эффективность и безопасность обоих препаратов у
детей. При этом более высокие значения внутрижелудочного
рН на фоне приема эзомепразола (5,9 против 4,88)
сопровождались повышением эффективности схемы эрадикации
при прочих равных условиях (83% против 75%).
Сравнительное исследование эффективности в зависимости от
длительности лечения подтвердило, что 7-дневная терапия не
достаточна для успешной эрадикации Н.pylori, но и
14-дневный курс, как рекомендует Маастрихт-3, может быть
излишним. 10-дневная тройная терапия с одним антибиотиком,
включавшая ИПП+Де-нол+амоксициллин оказалась
результативной в 75-83%.
Таким образом, тщательный подбор каждого компонента
эрадикационной схемы может быть залогом ее эффективности.
В условиях высокой резистентности Н.pylori к метронидазолу
и кларитромицину у детей в России может быть использована
схема с одним антибиотиком, включающая амоксициллин,
Де-нол и ингибитор протонной помпы, предпочтительно
эзомепразол. Оптимальная продолжительность лечения
составляет 10 дней. Схема хорошо переносится, удобна в
использовании, так как предусматривает двукратный прием
препаратов, и может быть примером усиления эффективности
терапии при одновременном снижении ее агрессивности.
Выводы:
1. У детей Санкт-Петербурга первичная
резистентность Н.pylori к кларитромицину очень высока и
составляет примерно 28%.
2. Схема 1 линии, рекомендованная Международным
консенсусом Маастрихт-3-2005 (ИПП+Кларитромицин+Метронидазол),
имеет низкую эффективность и плохую переносимость у детей.
3. Оптимальная продолжительность эрадикационной схемы
должна составлять 10 дней.
4. Эзомепразол (Нексиум) в эквивалентной дозе 2 мг/кг/с
хорошо переносится, сильнее подавляет желудочную секрецию,
чем омепразол, и в результате повышает эффективность
эрадикационной терапии.
5. Включение в схему Де-нола на 1 линии терапии
повышает ее результативность
6. Схема с одним антибиотиком – амоксициллином в
сочетании с ИПП и Де-нолом продолжительностью 10 дней
имеет высокую эффективность и хорошую переносимость.
Литература:
1. Lara L.F., Cisneros G., Gurney M. et al.
One-day quadruple therapy compared with 7-day triple
therapy for Helicobacter pylori infection. –
Arch.Intern.Med., 2003,v.163, p.2079-2084.
2. Veldhuyzen van Zanten S., Chiba N., Barkun A. et al. A
randomized trial comparing seven-day therapy for
eradication of Helicobacter pylori. – Can.J.Gastroenteriol.,
2003, v.17,p.533-538.
3. McLoughlin R., Racz I., O’Morain C. Therapy of
Helicobacter pylori. – Helicobacter, v.9,s.1,p.42-48.
4. Megraud F. Helicobacter pylori and macrolides.
In:Schonfeld W., Kirst H.A. macrolide antibiotics. –
Berlin, Berkhauser Verlag, 2002, p.243-260.
5. Mendz G.L., Megraud F. Is the molecular basis of
metronidazole resistance in microaerophilic organisms
understood? – Trends Microbiol.,2002, v.10, p.370.
6. Marais A., Bilardi C., Cantet F. et al.
Characterization of the genes rdxA and frxA involved in
metronidazole resistance in Helicobacter pylori. – Res.
Microbiol., 2003,v.154, p.137-144.
7. Pelerito A., Oleastro M., Labigne A. et al. Analysis of
Helicobacter pylori’s penicillin-binding proteins natural
polymorphism, therapeutical targets of the family of ?-lactam
antibiotics. – Helicobacter, 2003, v.8, p.394.
8. Koletzko S., Antos D., Richy F. et al. Antibiotic
resistance of Helicobacter pylori strains obtained from
children living in Europe: results of a prospective
multicenter study from 1999-2002.- J.Ped.Gastroentrol.Nutr.,
2004, v.39,s.1,p.s252.
9. Megraud F. H.pylori antibiotic resistance: prevalence,
impotance and advances in testing. – Gut, 2004, v.53,N 9,
p.1374-84.
10. Кудрявцева Л.В., Исаков В.А., Иваников И.О. и др.
Резистентность H.pylori к метронидазолу, кларитромицину и
амоксициллину в Москве, Санкт-Петербурге и Абакане в
2001г. – Педиатрия, 2002, №2 (приложение), с.61-63.
11. Fallone C.A. Epidemiology of the antibiotic resistance
of Helicobacter pylori – Can.J.Gastroenterol.,
2004,v.14,p.879-82.
12. Taneike I., Goshi S., Tamura Y. et al. Emergence of
claritromycin-resistant Helicobacter pylori with a high
prevalence in children compared with their parents. –
Helicobacter, 2002, V.7, p.297-305.
13. Glupczynski Y., Megroud F., Lopez-Brea M. et al.
European multicenter survey of in vitro antimicrobial
resistance in Helicobacter pylori. –
Eur.J.Clin.Microbiol.Infect.Dis., 2000, v.11, p.820-823.
14. Heep M., Kist M., Strobel S., et al. Secondary
resistance among 554 isolates of Helicobacter pylori after
failure of therapy. – Eur.J.Clin.Microbiol.Infect.Dis.,
2000, v.19, p.538-541.
15. European study group on antibiotic susceptibility of
Helicobacter pylori. Results of multicentre European
survey in 1991 of metronidazole resistance in Helicobacter
pylori. – Eur.J.Clin.Microbiol.Infect.Dis., 1992, v.9,
p.777-781.
16. Kist M., Glocker E., Wolf B. et al. ResiNet-A
nationwide German sentinel study on development and risk
factors of antimicrobial resistance in Helicobacter pylori.
– Helicobacter, 2003, v.8, p.465.
17. Корниенко Е.А. Клиника, диагностика и лечение
Helicobacter pylori-асоциированных гастродуоденальных
заболеваний у детей. –Автореф. дисс.докт., 1999, 32с.
18. Lerand F., Moum B., Ragnhildstveit E. et al.Simplified
10-day bismuth triple therapy for cure of Hrelicobacter
pylori infection: experience from clinical practice in a
population wiyh a high frequency of metronidazole
resistance. - Am.J.Gastroenterol., 1998, v.93,p.212-216.
19. Корниенко Е.А., Клочко О.Г. Выбор ингибиторов
протонной помпы при лечении детей. - Вопросы детской
диетологии, 2004, т.2,№1, с.48-49.
20. Исаков В.А., Домарадский И.В. Хеликобактериоз. – М.,
Медпрактика-М, 2003, 412с.
21. Mera R., Fontham E.T.H., Bravo L.E., et al. Longterm
follow up of patients treated for Helicobacter
pylori-infection. – Gut, 2005,v.54, p.1536-1540.
22. Falls G., Steininger H., Kranzlein J., et al.
Antigastric autoantibodies in Helicobacter pylori
infection. – Gut, 1997, v.41, p.619-623.
Статья опубликована на сайте
http://www.gastroscan.ru

