Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Системный подход в оценке показателей
периферической электрогастроэнтерографии у больных с осложненной
язвенной болезнью
С.А. Вавринчук, П.М. Косенко
Язвенная болезнь (ЯБ) желудка и двенадцатиперстной кишки (ДПК)
остаётся широко распространенным заболеванием, охватывающим до
10-15% трудоспособного населения. Нарушения моторно-эвакуаторной
функции (МЭФ) желудка и ДПК возникают у 10,0-56,3% больных ЯБ
[1,3,5,6,9] и до 65% случаев после её оперативного лечения
[3,8,12], что делает проблему своевременной диагностики и
профилактики послеоперационных нарушений МЭФ желудка не менее
актуальной.
Наиболее информативным современным методом изучения
функционального состояния желудка и кишечника является
периферическая электрогастроэнтерография (ПЭГЭГ) [2,4,7,10,11].
В отличие от электрогастрографии, ПЭГЭГ описывает
электрофизиологические изменения всех отделов ЖКТ с наличием
большого количества взаимосвязанных показателей, что
обусловливает необходимость использования системного подхода к
интерпретации данных ПЭГЭГ на основе современного многомерного
статистического анализа (МмСА).
Целью нашего исследования было улучшение качества оказания
хирургической помощи больным с осложнённой ЯБ путем
совершенствования электрофизиологической диагностики
моторно-эвакуаторных нарушений.
Материалы и методы
Нами обследовано 218 пациентов с осложнённой ЯБ желудка и ДПК.
Критериями включения пациентов в исследование было наличие
подтвержденных эндоскопическим и рентгенологическим методами
язвенного кровотечения и пилородуоденального стеноза (ПДС). В
исследование также были включены пациенты, оперированные по
поводу перфорации язвы ДПК и язвенного ПДС. Степень компенсации
ПДС определяли по Ю.М. Панцыреву и А.А. Гринбергу [6].
В соответствии с целью исследования все больные были нами
разделены на 3 основные группы. Первую группу составили 65
человек с ЯБ желудка и ДПК, осложненной кровотечением; вторую
группу – 57 больных с ЯБ, осложнённой ПДС и третью группу - 96
больных с осложненной ЯБ, которым были выполнены
органосохраняющие операции. Контрольную группу составили 28
практически здоровых людей (таблица 1).
Для электрофизиологической оценки состояния МЭФ желудка и
кишечника использовали ПЭГЭГ, которую выполняли аппаратом
”Гастроскан-ГЭМ” по стандартной методике [10].
Таблица 1. Распределение больных по
возрасту и полу
Группа больных
|
n
|
Средний возраст (M±m)
|
Пол
|
М
|
Ж
|
| n |
% |
n |
% |
| Контрольная группа |
28 |
40,7±4,1 |
12 |
42,8 |
16 |
57,2 |
| 1 |
65 |
48,0±2,6 |
39 |
60 |
26 |
40 |
| 2 |
57 |
55,3±2,1 |
39 |
68,4 |
18 |
31,6 |
| 3 |
96 |
53,1±1,8 |
67 |
69,8 |
29 |
30,2 |
| Всего |
246 |
50±1,38 |
157 |
63,8 |
89 |
36,2 |
При анализе ПЭГЭГ мы оценивали:
- суммарный уровень электрической активности (Ps) органов
ЖКТ;
- электрическую активность (ЭА) по отделам ЖКТ (Pi);
- процентный вклад каждого частотного спектра в суммарный
спектр (Pi/Ps) (%);
- коэффициент ритмичности (Критм), который характеризует
наличие и характер пропульсивных сокращений гладкомышечных
структур для каждого отдела ЖКТ;
- коэффициент соотношения Pi/P(i+1) - отношение ЭА
вышележащего отдела к нижележащему.
Для оценки степени компенсации ПДС, нами были дополнительно
предложены относительные показатели:
- «показатель компенсации ЭА желудка», который представляет
собой отношение значений стимулированного Pi желудка к его
базальному значению и характеризует ЭА желудка;
- «показатель компенсации перистальтической активности
желудка», который представляет собой отношение значений
стимулированного Критм желудка к его базальному значению и
характеризует перистальтическую активность желудка.
Многомерный статистический анализ (МмСА) показателей ПЭГЭГ
включал в себя сравнение средних значений показателей ПЭГЭГ в
независимых группах с расчетом непараметрического критерия
Манна-Уитни, кластерный анализ в виде иерархической
кластеризации, дискриминантный анализ и метод логистической
регрессии.
Анализ полученных данных выполнялся в статистическом пакете
Statsoft Statistica 8.0.
Результаты исследования
Сравнение средних значений показателей ПЭГЭГ больных первой
группы с контрольными значениями выявило достоверное (p<0,05)
снижение у больных с язвенным дуоденальным кровотечением ЭА
желудка с одновременным повышением ЭА толстой кишки. Нами так же
было отмечено возрастание значений базального и стимулированного
Pi/P(i+1) ДПК/тощая кишка, что свидетельствовало о
дискоординации моторики данного сегмента кишечника.
У больных с желудочной локализацией язвы сравнение
показателей ПЭГЭГ с контрольными значениями выявило достоверные
различие по 14 показателям, преимущественно за счет изменения
показателей ЭА и коэффициента соотношения отделов ЖКТ.
Для проведения дискриминантного анализа группирующим
признаком была определена локализация язвы.
Статистически значимыми признаками оказались:
- базальные значения Ps, Pi/Ps желудка, подвздошной и
толстой кишки; Pi/P(i+1) тощая/подвздошная кишка и Pi/P(i+1)
подвздошная/толстая кишка; Критм толстой кишки;
- стимулированные значения Pi/Ps тощей кишки; Pi/P(i+1)
тощая/ подвздошная кишка, Критм желудка.
Если при сравнении средних значений показателей ПЭГЭГ
наибольшее количество достоверных различий в сравнении с
контрольной группой было выявлено у больных с желудочной
локализацией язвы, то по данным дискриминантного анализа эти
пациенты, наоборот, классифицировались как здоровые в 23%
случаев, а больные с дуоденальной локализацией язвы – только в
5,1% случаев (таблица 2).
Таблица 2. Прогностическая точность
изменений моторики ЖКТ в зависимости от локализации источника
язвенного кровотечения по результатам дискриминантного анализа
| Матрица переклассификации |
Наблюдаемое
распределение |
Предсказанное
распределение |
Группы пациентов
|
Группы пациентов
|
% правильной
классификации |
| ЯБ ДПК |
ЯБ желудка |
Контрольная
группа |
| ЯБ ДПК |
n=39 |
37 |
0 |
2 |
94,8 |
| ЯБ желудка |
n=26 |
2 |
18 |
6 |
69,2 |
| Контрольная группа |
n=28 |
0 |
0 |
28 |
100,0 |
| Всего |
n=93 |
39 |
18 |
36 |
88,8 |
Выявление дискриминантным методом более выраженные нарушения
МЭФ желудка у больных с ЯБ ДПК, осложнённой кровотечением,
по-нашему мнению, объясняются его способностью оценивать не
только изменения отдельных показателей ПЭГЭГ, но и их
корреляционные взаимосвязи с другими показателями.

Рисунок 1. Распределение групп пациентов с
ЯБ, осложненной кровотечением, по показателям ПЭГЭГ в
зависимости от локализации язвы на основании дискриминантного
анализа
Таким образом, созданная на основе дискриминантного анализа
электрофизиологическая модель нарушений МЭФ желудка и ДПК у
больных с ЯБ, осложнённой кровотечением, в зависимости от
локализации язвы показала, что данные группы достоверно
отличаются по 10 показателям ПЭГЭГ со средней точностью модели
для прогнозирования распределения пациентов в ту или иную группу
88,8% (рисунок 1).
Анализ средних значений показателей ПЭГЭГ у больных 2-й
группы показал характерные [10] изменения в виде умеренного (p>0,05)
возрастания ЭА и перистальтической активности желудка у больных
с компенсированным ПДС, статистически значимого (p<0,05)
возрастания базальной и стимулированной ЭА и перистальтической
активности желудка у больных с субкомпенсированным ПДС, а также
достоверного (p<0,05) снижения стимулированной ЭА и
перистальтической активности у больных с декомпенсированным ПДС.
Традиционно все пациенты с ПДС разделяются по степени его
компенсации на компенсированный, суб- и декомпенсированный
стенозы [6].
Однако результаты до- и послеоперационного обследования
пациентов с субкомпенсированным ПДС, свидетельствуют об их
неоднородности по характеру изменений МЭФ желудка, что,
по-нашему мнению, связано с наличием в этой наиболее
многочисленной группе пациентов переходных типов нарушения
моторики от компенсации к её декомпенсации, которые не
обнаруживаются стандартным методом сравнения средних показателей
ПЭГЭГ.
Для выявления этих переходных типов компенсации моторики
желудка мы использовали кластерный анализ, в который были
включены 40 показателей ПЭГЭГ 24 пациентов с субкомпенсированным
ПДС.
В результате кластеризации были выявлены 2 группы больных
(рисунок 2). В первую группу вошли 10 (41,6%) пациентов, которых
мы соответственно выявленному характеру изменений
электрофизиологических показателей условно обозначили как группу
больных с гипомоторным типом ПДС, и во вторую группу - 14
(58,3%) пациентов, которых мы также условно обозначили как
группу больных с гипермоторным типом ПДС.
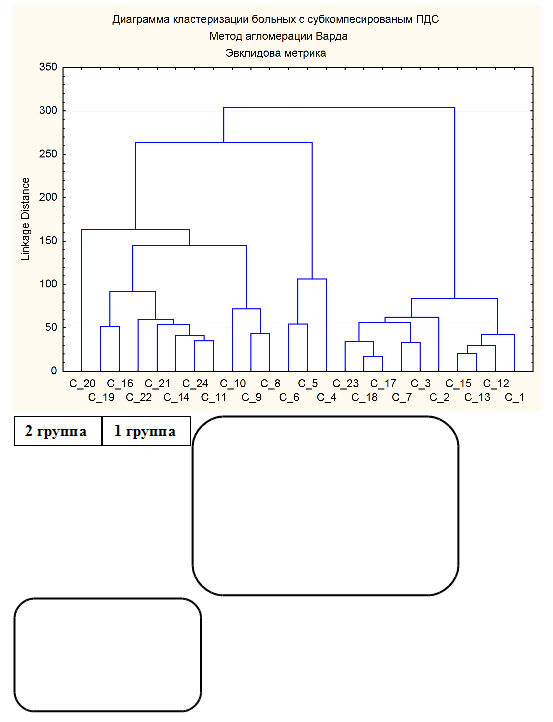
Рисунок 2. Дендрограмма объединения в
кластеры пациентов с субкомпенсированным ПДС
Анализ средних показателей ПЭГЭГ у больных с гипермоторным
типом субкомпенсированного ПДС показал наличие у них крайней
степени компенсации моторной функции желудка, что проявлялось
умеренным (p>0,05) повышением базальной ЭА и перистальтической
активности желудка и кишечника со значительным их возрастанием
после пищевой стимуляции (p<0,05).
Показатели ПЭГЭГ у больных с гипомоторным типом
субкомпенсированного ПДС отражали уже начальные проявления
декомпенсации моторики желудка, что проявлялось повышением
базального тонуса желудка и его перистальтический активности (p<0,05)
со снижением этих показателей после пищевой стимуляции,
обусловленное развитием недостаточности нервно-мышечного
аппарата желудка и усугублением его двигательных расстройств.
На основе дискриминантного анализа нами была создана
электрофизиологическая модель моторно-эвакуаторных нарушений у
больных с язвенным ПДС, включающая выявленные переходные типы
нарушения моторики желудка, а так же возрастные особенности
значений ПЭГЭГ.
В электрофизиологическую модель вошло 23 показателя ПЭГЭГ, из
которых статистически значимыми оказались 17 (таблица 3).
Таблица 3. Показатели модели определения
степени тяжести ПДС по данным ПЭГЭГ
Показатели модели
|
Показатели
дискриминантного анализа |
Лямбда
Уилкса |
Частичная
лямбда |
F
статистика |
p |
Tolerance |
1-Toler. (R-Sqr.) |
Ps (mB)
|
Базал. |
0,0099 |
0,5628 |
5,0494 |
p<0,01 |
0,0001 |
0,9999 |
| Стим. |
0,0107 |
0,5211 |
5,9729 |
p<0,01 |
0,0074 |
0,9993 |
Pi (mB)
|
желудок базал. |
0,0091 |
0,6115 |
4,1279 |
p<0,01 |
0,0006 |
0,9925 |
| подвзд. кишка базал. |
0,0113 |
0,4932 |
6,6770 |
p<0,01 |
0,0007 |
0,9992 |
| Подвзд. кишка стим. |
0,0112 |
0,5001 |
6,4959 |
p<0,01 |
0,0055 |
0,9944 |
| тостая кишка базал. |
0,0104 |
0,5388 |
5,5637 |
p<0,01 |
0,0004 |
0,9995 |
Pi/Ps (%)
|
желудок базал. |
0,0096 |
0,5846 |
4,6181 |
p<0,01 |
0,0212 |
0,9787 |
| желудок стим |
0,0077 |
0,7250 |
2,4646 |
p<0,05 |
0,0984 |
0,9015 |
| ДПК стим. |
0,0078 |
0,7156 |
2,5828 |
p<0,05 |
0,0439 |
0,9560 |
| тощая кишка стим. |
0,0078 |
0,7144 |
2,5980 |
p<0,05 |
0,0182 |
0,9817 |
| подвзд. кишка базал. |
0,0083 |
0,6746 |
3,1344 |
p<0,05 |
0,0863 |
0,9136 |
| подвзд. кишка стим. |
0,0089 |
0,6257 |
3,8881 |
p<0,05 |
0,0346 |
0,9653 |
| толстая базал. кишка |
0,0103 |
0,5414 |
5,5043 |
p<0,01 |
0,0122 |
0,9877 |
Pi/p(i+1)
|
ДПК/тощая кишка базал. |
0,0095 |
0,5871 |
4,5709 |
p<0,01 |
0,0808 |
0,9191 |
| ДПК/тощая кишка стим. |
0,0071 |
0,7811 |
1,8208 |
p<0,05 |
0,1112 |
0,8887 |
| тощая/подвзд. стим. |
0,0081 |
0,6869 |
2,9619 |
p<0,05 |
0,0452 |
0,9547 |
| подвзд./толстая базал. |
0,0095 |
0,5885 |
4,5434 |
p<0,01 |
0,0259 |
0,9740 |
Критм.
|
желудка базал. |
0,0071 |
0,7885 |
1,7429 |
p<0.05 |
0,0065 |
0,9934 |
| желудка стим. |
0,0104 |
0,5384 |
5,5727 |
p<0.01 |
0,0073 |
0,9926 |
| ДПК базал. |
0,0107 |
0,5239 |
5,9049 |
p<0.01 |
0,0162 |
0,9837 |
| тощая базал. |
0,0069 |
0,8112 |
1,5119 |
p<0.05 |
0,0087 |
0,9912 |
| подвзд. кишка стим. |
0,0102 |
0,5470 |
5,3815 |
p<0.01 |
0,0061 |
0,9938 |
| толстая базал. |
0,0129 |
0,4322 |
8,5370 |
p<0,01 |
0,0044 |
0,9955 |
Примечание: 17 Шагов, переменных в модели 23, число групп –
5. Лямбда Уилкса: 0,03502 approx. F (60,193)=4,3861; p< 0,0000
Общий процент правильной классификации наблюдений в
соответствующие группы составил 96,2% (таблица 4, рисунок 3).
Таблица 4. Точность диагностики степени ПДС
на основе показателей ПЭГЭГ, полученных в результате
дискриминантного анализа
| Матрица переклассификации |
Наблюдаемое распределение
|
Предсказанное
распределение |
| Группы пациентов |
Группы пациентов
|
Контрольная группа
|
ПДС
|
% правильной
классификации
|
Компенси-рованный
|
Субкомпенсированный |
Декомпенси-рованный
|
| гипермоторн. тип |
гипомоторн. тип |
ПДС
|
Компенсированный
|
0 |
25 |
0 |
0 |
0 |
100 |
Суб
компенси-рованный
|
Гипермоторн. тип |
0 |
0 |
14 |
0 |
0 |
100 |
| Гипомоторн. тип |
0 |
0 |
0 |
10 |
0 |
100 |
Декомпенсированный
|
1 |
0 |
0 |
0 |
7 |
90 |
| Контрольная группа |
0 |
0 |
1 |
0 |
9 |
90 |
| Всего |
1 |
25 |
15 |
10 |
16 |
96,2 |
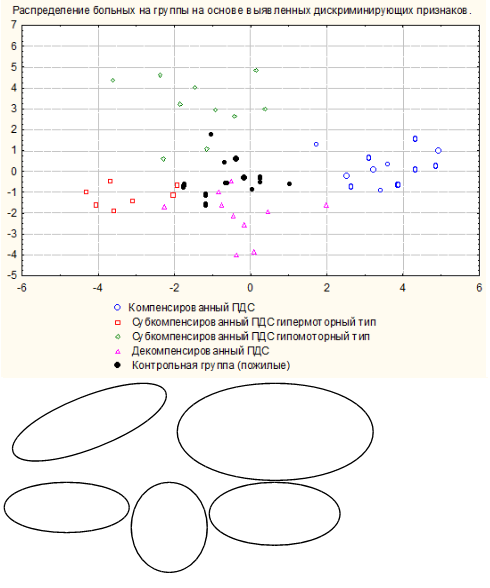
Рисунок 3. Распределение больных ЯБ,
осложненной ПДС, по показателям ПЭГЭГ на основании
дискриминантного анализа с учётом возрастных значений ПЭГЭГ
Для подтверждения соответствия выявленных нами
моторно-эвакуаторных нарушений ЖКТ степеням компенсации ПДС был
применён метод многофакторной логистической регрессии. Для
построения логистических уравнений использовались 40 предикторов
(базальные и стимулированные показатели ПЭГЭГ) в разных
сочетаниях с их пошаговым исключением из модели.
В созданную модель вошло 27 показателей ПЭГЭГ. Её общая
прогностическая точность составила 88,8%.
Таким образом, результаты метода многофакторной логистической
регрессии полностью подтвердили данные дискриминантного анализ о
соответствии выявленных моторно-эвакуаторных нарушений ЖКТ
уточнённым нами степеням компенсации ПДС.
Системный анализ показателей ПЭГЭГ у больных 3-й группы
показал, что после ушивания ПЯ ДПК средние значения показателей
ПЭГЭГ соответствовали субкомпенсированному ПДС с нарушением
пропульсивной перистальтики и начальными признаками
декомпенсации моторики желудка. Это проявлялось статистически
значимым возрастанием базальной ЭА и перистальтической
активности желудка с их снижением после пищевой стимуляции и
задержкой появления признаков начала эвакуации пищи из желудка в
ДПК до 20±5 минуты исследования.
У больных после радикальной дуоденопластики (РДП), которая
устраняла саму язву, сочетанные язвенные осложнения и
перидуоденальные рубцовые сращения, лежащие в основе нарушения
МЭФ желудка, были отмечены возрастание стимулированных
показателей Pi желудка и ДПК, коэффициента соотношения Pi/P(i+1)
желудок/ДПК, восстановление физиологического трёхфазного
характера стимулированной электрофизиологической кривой и
нормализация времени эвакуации из желудка в ДПК. Эти изменения
указывали на восстановление пропульсивной ЭА в области
дуоденогастрального перехода.
Выявленные нами изменения показателей ПЭГЭГ после ушивания ПЯ
ДПК и РДП так же были подвергнуты дискриминантному анализу.
Статистически значимыми для оценки выявленных методом ПЭГЭГ
различий послеоперационных моторно-эвакуаторных изменений
оказались базальные значения Ps, Pi подвздошной и толстой кишки;
Pi/Ps желудка и толстой кишки; Pi/P(i+1) тощей/подвздошной и
подвздошной/толстой кишки; Критм подвздошной кишки, а также
стимулированные значения Pi и Pi/Ps ДПК, Pi/Ps толстой кишки, Pi/P(i+1)
желудка/ДПК, Критм желудка и подвздошной кишки. Статистически
значимым оказался и показатель компенсации перистальтической
активности желудка.
Это подтвердило наличие статистически значимых различий
значений показателей ПЭГЭГ здоровых лиц и в группах пациентов
после ушивания ПЯ ДПК и РДП и определило показатели ПЭГЭГ,
влияющие на распределение больных по характеру
моторно-эвакуаторных нарушений в каждую из групп.
Результаты дискриминантного анализа показали высокую степень
различия показателей ПЭГЭГ после ушивания ПЯ ДПК и РДП (рисунок
4).
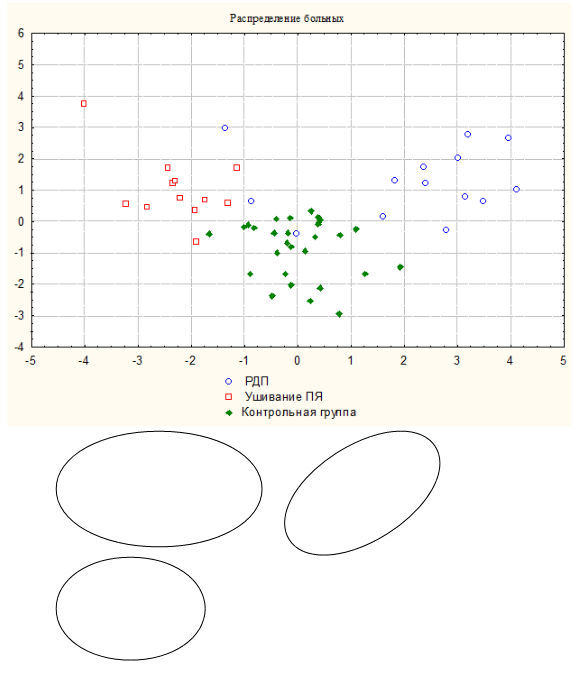
Рисунок 4. Распределение больных с ПЯ ДПК
после ушивания ПЯ и РДП и лиц контрольной группы по показателям
ПЭГЭГ на основании дискриминантного анализа
Таблица 5. Наблюдаемое и предсказанное по
данным ПЭГЭГ распределение здоровых лиц и больных с ПЯ ДПК после
ушивания ПЯ и РДП
| Матрица переклассификации |
Наблюдаемое распределение
|
Предсказанное
распределение |
Группы
пациентов
|
Группы пациентов
|
% правильной
классификации
|
Контрольная
группа |
После ушивания
ПЯ ДПК |
После
РДП |
| Контрольная группа |
n=28 |
28 |
0 |
0 |
100 |
| После ушивания ПЯ ДПК |
n=26 |
2 |
24 |
0 |
91,6 |
| После РДП |
n=38 |
6 |
2 |
30 |
78,5 |
| Всего |
n=92 |
92,5 |
30 |
26 |
92,5 |
Наличие межгрупповых различий позволило создать
электрофизиологическую модель моторно-эвакуаторных нарушений у
больных с ПЯ ДПК после ушивания ПЯ и РДП с высокой
прогностической эффективностью, достигающей 92,3% (таблица 5).
У больных ПЯ ДПК после РДП большинство значений показателей
ПЭГЭГ было ближе к контрольным значениям, и они в 21,5% случаев
классифицировались как здоровые, в то время как больные после
ушивания ПЯ были отнесены в группу здоровых лишь в 8,4% случаев.
Полученные нами данные были учтены в практической работе. Мы
отказались от ушивания ПЯ ДПК в пользу выполнения РДП, что
сократило количество послеоперационных осложнений на 24% и
позволило избежать повторных операций по поводу
послеоперационных нарушений МЭФ желудка.
У больных с декомпенсированным ПДС на фоне нарушения
нервно-рефлекторных связей желудка и кишечника в
послеоперационном периоде развивались наиболее тяжелые формы
моторно-эвакуаторных нарушений, с развитием атонии желудка после
изолированной РДП и атонии культи желудка после его резекции.
Данные о состоянии моторной функции желудка у больных с ПДС
после селективной проксимальной ваготомии (СПВ) в сочетании с
дренирующими операциями носят разноречивых характер [5,8,12].
Сообщения об электрофизиологической оценке желудка методом ПЭГЭГ
после РДП в сочетании СПВ в литературе отсутствуют.
Системный анализ показателей ПЭГЭГ больных 3 группы после РДП
в сочетании с СПВ показал что, у больных с гипермоторным типом
субкомпенсированного ПДС отмечено статистически значимое
снижение стимулированной ЭА и перистальтической активности
желудка, что по-нашему мнению было обусловлено денервацией
желудка. При этом базальные значения ЭА желудка соответствовали
дооперационному уровню, что указывало на отсутствие влияния на
неё СПВ. У больных данной группы в послеоперационном периоде
отсутствовали признаки послеоперационного гастростаза и, по
данным комплексного обследования, уже через 2 недели после
операции отмечалась нормализация размеров и моторики желудка.
У больных с гипомоторным типом субкомпенсированного ПДС,
напротив, было отмечено снижение базальной ЭА желудка
стимулированной ЭА и перистальтической активности желудка с ещё
большим их снижением после пищевой стимуляции. Снижение более
высоких, чем у пациентов с гипермоторным типом ПДС уровня
базальной ЭА желудка мы связываем с восстановлением пассажа
желудочного содержимого после РДП. В этой группе больных имелись
клинические, рентгенологические и электрофизиологические
признаке послеоперационного гастростаза с восстановлением
размеров и МЭФ желудка только через 6-7 месяцев после операции.
Выявленные различия показателей ПЭГЭГ у больных гипер- и
гипомоторным типом субкомпенсированного ПДС после РМД+СПВ были
так же проверены методом дискриминантного анализа..
В созданную модель послеоперационных моторно-эвакуаторных
нарушений вошло 13 показателей ПЭГЭГ. Статистически значимыми
оказались базальный и стимулированный Pi желудка, базальный Pi
тощей кишки, базальный Pi/P(i+1) тощая/подвздошная кишка,
базальный Критм желудка и стимулированный Критм подвздошной
кишки.
В результате анализа было выявлено, что около 30% больных
обеих групп после РДП+СПВ не имели достоверных отличий по
показателям ПЭГЭГ от контрольной группы что позволило их
классифицировать как здоровых (рисунок 5).

Рисунок 5. Распределение больных с
различными типами субкомпенсированного ПДС после РДП+СПВ по
показателям ПЭГЭГ
У 71,4% больных с субкомпенсированным ПДС по гипермоторному
типу и 70,0% больных с субкомпенсированным ПДС по гипомоторному
типу после операции имелись значимые различия
электрофизиологических показателей с классификацией их в разные
группы. Все пациенты контрольной группы были классифицированы
правильно (100%).
Общий процент правильной классификации наблюдений в
соответствующие группы составил 86,5% (таблица 6).
Таблица 6. Результаты дискриминантного
анализа показателей ПЭГЭГ у больных после РДП+СПВ
| Матрица переклассификации |
Наблюдаемое распределение
|
Предсказанное
распределение |
Группы пациентов
|
Группы пациентов
|
Субкомпенсированный ПДС
|
Контрольная
группа
|
% правильной
классификации
|
| Гипермоторный тип |
Гипомоторный тип |
Субкомпенси-
рованный ПДС
|
Гипермоторный тип |
10 |
0 |
4 |
71,4 |
| Гипомоторный тип |
0 |
7 |
3 |
70,0 |
Контрольная группа
|
0 |
0 |
28 |
100 |
Всего
|
10 |
7 |
35 |
86,5 |
Таким образом, системный анализ показателей ПЭГЭГ подтвердил
наличие достоверных различий в характере и продолжительности
компенсации послеоперационных моторно-эвакуаторных нарушений у
пациентов с гипермоторным и гипомоторным типом
субкомпенсированного ПДС после РДП в сочетании с СПВ.
Выводы
Системный подход к анализу показателей ПЭГЭГ с использованием
МмСА позволил выявить изменения моторики ЖКТ у больных с ЯБ,
осложнённой кровотечением, в зависимости от локализации язвы, с
наибольшими её изменениями у больных с дуоденальной локализацией
язвы.
Применение МмСА показателей ПЭГЭГ у больных с ЯБ, осложнённой
субкомпенсированным ПДС, позволило выявить неоднородные по
характеру моторно-эвакуаторных нарушений группы больных с
наличием переходных типов от компенсации моторики желудка (гипермоторный
тип) к её декомпенсации (гипомоторный тип).
Дискриминантным методом и методом многофакторной
логистической регрессии подтверждено, что сохранение язвы ДПК,
сочетанных язвенных осложнений, перидуоденальных рубцовых
сращений и деформация пилородуоденальной зоны после ушивания ПЯ
ДПК приводит к моторно-эвакуаторным нарушениям, соответствующим
субкомпенсированному ПДС, а их устранение и пластическое
восстановление ДПК при РДП восстанавливает моторно-эвакуаторную
функцию желудка.
Системный подход к анализу данных ПЭГЭГ позволил выявить и
подтвердить зависимость моторики желудка у больных с ЯБ,
осложнённой субкомпенсированным ПДС после РДП в сочетании с СПВ
от её дооперационного состояния (гипермоторный и гипомоторный
тип).
У больных с субкомпенсированным ПДС по гипермоторному типу
отмечено снижение стимулированной электрической и
перистальтической активности желудка с сохранением его базальной
ЭА на дооперационном уровне, что сопровождалось ранним (до 2-х
недель) восстановлением МЭФ желудка.
У больных с гипомоторным типом субкомпенсированного ПДС
выявлено послеоперационное снижение базальной и стимулированной
электрической и перистальтической активности желудка с
признаками послеоперационного гастростаза и длительным (до 6-7
месяцев) восстановлением МЭФ желудка.
Системный подход в оценке данных ПЭГЭГ у больных с
осложнённой ЯБ повысил её диагностическую значимость, позволил
создать диагностические модели моторно-эвакуаторных нарушений
для каждого из этих осложнений и оценить их прогностическую
точность. Учёт возрастных особенностей значений показателей
ПЭГЭГ повысил её диагностическую ценность.
Литература:
- Ермолаев И.А. Сравнительные результаты различных видов
оперативного лечения при осложненной дуоденальной язве
(показания, методы, осложнения, ближайшие и отдаленные
результаты): автореф. дис. . канд. мед. наук.
–Санкт-Петербург, 2005. -24с.
- Использование накожной электрогастрографии для оценки
состояния желудочно-кишечного тракта/ Ворновицкий Е.Г.,
Фельдштейн И.В./ Ворновицкий Е.Г., Фельдштейн И.В.// Бюллетень
экспериментальной биологии и медицины.- 1998.- Том 126.- N11.
С.597-600.
- Майстренко Н.А., Мовчан К.Н. Хирургическое лечение язвы
двенадцатиперстной кишки. - СПб.: Гиппократ, 2000. - 360 с.
- Нотова О.Л. Оценка моторной деятельности желудка и
различных отделов кишечника по данным периферической
полиэлектрографии: Дис.канд.мед.наук.-М., 1987.-271 С.
- Оноприев В.И. Новые концепции, тактика и технологии
хирургического лечения осложнённых дуоденальных язв // Вестник
хирургической гастроэнтерологии. — 2006. — №1. — С. 11—16
- Панцырев Ю.М., Гринберг А.А. Ваготомия при осложнённых
дуоденальных язвах. — М.: Медицина, 1979. - 159 с.
- Периферическая электрогастроэнтерография в диагностике
нарушений моторно-эвакуаторной функции желудочно-кишечного
тракта/Ступин В.А., Смирнова Г.О., Баглаенко М.В., Силуянов
СВ. // Лечащий врач.- 2005.- №2. - С 60-62.
- Рудик А. А. Сравнительные результаты различных видов
оперативного лечения при осложнённой дуоденальной язве [Текст]
: дис. … д-ра мед. наук / А. А. Рудик. – Хабаровск, 2001. –
331 с.
- Синченко Г.И. Курыгин А.А. Сочетанные осложнения язвы
двенадцатиперстной кишки – СПб: Фолиант,2007.-192с.
- Смирнова Г.О. Периферическая электрогастроэнтерография в
клинической практике. - Пособие для врачей / под ред. проф.
В.А. Ступина.- М.: ИД «Медпрактика-М».- 2009.- 20 С.
- Теоретические предпосылки и экспериментальное обоснование
использования электрогастроэнтерографии / Н.С. Тропская, В.А.
Васильев,Т.С. Попова // Российский журнал гастроэнтерологии,
гепатологии, колопроктологии. - 2005. - №5 . - С. 82-87.
- Kennedy, T. Duodenoplasty with Proximal gastric vagotomy /
T. Kennedy // Ann. roy. Coll. Surg. Engl. - 1976. - Vol. 58. -
P. 144-146.
Статья опубликована на сайте
http://www.gastroscan.ru

