Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Лечение нарушений липидного обмена при сахарном диабете 2
типа
И. В. Глинкина, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
Сердечно-сосудистые заболевания (ССЗ), распространенность которых среди
пациентов с сахарным диабетом (СД) 2 типа более чем в 4 раза превышает таковую у
лиц без данного заболевания, являются причиной смерти 70–80% больных. Столь
высокая распространенность сердечно-сосудистой патологии среди пациентов с СД 2
типа обусловлена сочетанием как «классических», присущих популяции в целом, так
и связанных именно с СД факторов риска развития атеросклероза. Среди первых
наибольшую значимость представляют нарушения липидного обмена, которые, по
данным литературы, диагностируются у 50–97% пациентов, а также артериальная
гипертензия, ожирение, курение и повышенная активность свертывающей системы
крови. Среди вторых — инсулинорезистентность, гиперинсулинемия и гипергликемия
[11]. В ходе исследования UK Prospective Diabetes Study (UKPDS) было показано,
что достижение нормогликемии достоверно снижает риск развития микроваскулярных,
но не макроваскулярных осложнений СД 2 типа, в то время как снижение
артериального давления достоверно уменьшает частоту развития макрососудистых
катастроф, а повышение уровня холестерина достоверно ее увеличивает [15]. Таким
образом, наиболее оправданной стратегией ведения пациентов с СД 2 типа является
стратегия АВС, предложенная Национальной образовательной программой по диабету:
диабетологи и больные СД должны уделять внимание не только контролю гликемии
(«А» — HbA1c) и артериального давления («В» — blood pressure), но и уровню
липидов крови («С» — cholesterol) [32].
Патогенез нарушений липидного обмена при СД 2 типа.
Основными характеристиками дислипидемии при СД 2 типа являются повышение уровня
триглицеридов в составе липопротеинов очень низкой плотности (ЛПОНП) и снижение
уровня холестерина липопротеинов высокой плотности (ХС ЛПВП). Концентрация
холестерина липопротеинов низкой плотности (ХС ЛПНП) у больных СД практически не
отличается от таковой у лиц без данного заболевания, однако у пациентов с СД 2
типа преобладает фракция мелких плотных ЛПНП, обладающих повышенной
атерогенностью вследствие высокой способности к окислению. Количественные
изменения липидного спектра могут встречаться изолированно, но чаще они
сочетаются и носят название липидной триады или атерогенной дислипидемии.
Основной причиной гипертриглицеридемии при СД 2 типа является низкая
чувствительность висцеральной жировой ткани к антилиполитическому действию
инсулина, что ведет к повышенному липолизу, поступлению большого количества
свободных жирных кислот в портальный кровоток и, в сочетании с гиперинсулинемией,
повышению синтеза триглицеридов и ЛПОНП печенью. Кроме этого, у больных СД 2
типа при гипергликемии снижена активность эндотелиальной липопротеинлипазы,
ответственной за катаболизм триглицеридов и ЛПОНП, что усугубляет данное
нарушение. Снижение уровня ХС ЛПВП при СД 2 типа обусловлено повышением
активности печеночной липопротеинлипазы и ускоренным катаболизмом ХС ЛПВП.
Помимо количественных, при СД 2 типа имеют место также качественные изменения
липидного спектра: при гипергликемии возрастает доля гликированных ЛПНП, в том
числе мелких плотных ЛПНП, обладающих повышенной атерогенностью в связи с
высокой способностью к окислению и накоплению в артериальной стенке, а также к
замедленному клиренсу и длительному нахождению в плазме. В свою очередь,
гликирование и окисление ЛПВП также ведет к снижению их антиатерогенных свойств.
Развитие у пациентов диабетической нефропатии усугубляет уже имеющееся повышение
уровня триглицеридов и снижение уровня ХС ЛПВП. Изменение любого показателя
липидного спектра ведет к увеличению сердечно-сосудистого риска у пациентов с СД
2 типа (табл. 1), он значительно возрастает при комбинированной дислипидемии
[3].
Диагностика и лечение нарушений липидного обмена при СД 2 типа.
Американская диабетологическая ассоциация (АДА) рекомендует исследование
липидного спектра, включающего общий холестерин (ОХС), триглицериды, ХС ЛПНП, ХС
ЛПВП, в момент установления диагноза СД 2 типа. При отсутствии нарушений
липидного обмена повторное исследование проводится ежегодно. У пациентов,
которые остаются в группе низкого риска развития ССЗ, исследование липидного
спектра может проводиться 1 раз в 2 года [10].
Согласно рекомендациям АДА, основной целью лечения дислипидемии при СД 2 типа
является снижение уровня ХС ЛПНП < 100 мг/дл (2,6 ммоль/л) [3]. ХС ЛПНП выбран в
качестве основного параметра липидного спектра в связи с тем, что, по данным
крупномасштабных проспективных исследований, именно снижение уровня ХС ЛПНП
ассоциировано с достоверным снижением возникновения сердечно-сосудистых событий
и смертности от них. АДА рекомендует назначение пациентам с СД 2 типа только
немедикаментозной терапии при уровне ХС ЛПНП 100–129 мг/дл и отсутствии ССЗ (табл.
2) сроком на 3–6 мес с повторным исследованием липидного спектра каждые 6
нед и окончательным решением вопроса о назначении медикаментозной терапии. При
уровне ХС ЛПНП ≥ 130 мг/дл у больных СД 2 типа без ССЗ одновременно с
немедикаментозной терапией назначается медикаментозная. Такая же тактика
рекомендована АДА при уровне ХС ЛПНП > 100 мг/дл у пациентов с СД 2 типа и
наличием ССЗ (табл. 2) [3].
Цели и тактика лечения дислипидемии в зависимости от
уровня ХС ЛПНП (мг/дл) и сердечно-сосудистого риска (АДА, 2002)

Для ХС ЛПВП рекомендованы целевые значения > 45 мг/дл (1,15 ммоль/л), причем
для женщин этот показатель может быть даже > 55 ммоль/л с учетом того, что
женщины имеют более высокий уровень ХС ЛПВП, чем мужчины. Для триглицеридов
желательный уровень < 150 мг/дл (1,7 ммоль/л) [3]. При нормальном уровне ХС ЛПНП
и отклонении от нормальных значений ХС ЛПВП и/или триглицеридов у пациентов с СД
2 типа и ССЗ немедикаментозная и медикаментозная терапия назначаются
одновременно, при отсутствии ССЗ — в течение 3–6 мес показана только
немедикаментозная терапия, решение о назначении медикаментозной терапии
принимается после повторных исследований липидного спектра.
Немедикаментозная терапия заключается в изменении образа жизни,
предполагающем отказ от курения, расширение физической активности, модификацию
питания.
Адекватная физическая активность ведет к снижению инсулинорезистентности и
веса за счет уменьшения количества висцеральной жировой клетчатки, что
сопровождается снижением уровня триглицеридов и повышением уровня ХС ЛПВП, а
также умеренным снижением уровня ХС ЛПНП. С целью снижения веса АДА рекомендует
аэробные физические нагрузки длительностью 20–45 мин минимум 3 раза в неделю
[4].
Модификация питания с целью снижения веса и коррекции нарушений липидного
обмена, согласно рекомендациям АДА, заключается в снижении доли насыщенных жиров
и увеличении в рационе доли моно- или полиненасыщенных жиров или углеводов [5].
Диета, рекомендованная АДА при дислипидемии, включает: жиры — 25–35%
суточного калоража (насыщенные — < 7% суточного калоража, полиненасыщенные — 10%
суточного калоража, мононенасыщенные — > 20% суточного калоража); углеводы —
50–60% суточного калоража; белки — 15% суточного калоража; клетчатка — 20–30
мг/день; холестерин — < 200 мг/день.
Однако пациентам с СД 2 типа при наличии избыточного веса такая диета
показана еще до выявления нарушений липидного обмена, что не позволяет
рассчитывать на высокую эффективность модификации питания с целью коррекции
нарушений липидного спектра у большинства пациентов.
Медикаментозная терапия. Анализ результатов многоцентровых
рандомизированных плацебо-контролируемых исследований, включавших группы больных
СД 2 типа, позволяет сделать вывод о положительном эффекте применения
гиполипидемической терапии в качестве как первичной, так и вторичной
профилактики ССЗ у пациентов с СД 2 типа. В трех исследованиях — Cholesterol and
Recurrent Events Study (CARE), Scandinavian Simvastatin Survival Study (4S) и
Long-term Intervention of Pravastatin on Ischaemic Disease (LIPID) — изучалось
применение статинов у пациентов с СД 2 типа и ИБС. Использование данных
препаратов позволило снизить уровень ЛПНП на 28, 36 и 25% соответственно и
уровень сердечно-сосудистых событий на 25% (р = 0,05), 55% (р = 0,002) и 19%
(недостоверно) соответственно [7, 8, 12, 13]. Сходный результат — снижение
сердечно-сосудистых событий на 24% при увеличении уровня ХС ЛПВП — получен в
ходе исследования Veterans Affairs Cooperative Studies Program HDL-C
Intervention Trial (VA-HIT) при использовании гемфиброзила. Heart Protection
Study (HPS) — единственное на сегодняшний день исследование по первичной
профилактике ишемической болезни сердца (ИБС) при применении гиполипидемической
терапии — показало достоверное снижение частоты коронарных событий при лечении
симвастатином. В исследовании HPS 67% больных СД не имели в анамнезе ИБС, и
именно у этой группы преимущества терапии были существенно более выраженными,
чем у больных СД с ИБС в анамнезе [9]. Данные факты свидетельствуют о
необходимости коррекции нарушений липидного обмена у пациентов с СД 2 типа.
В настоящее время существуют четыре группы препаратов, оказывающих влияние на
липидный спектр: ингибиторы 3-гидрокси-3-метилглутарил-коэнзимА-редуктазы
(ингибиторы ГМГ-КоА-редуктазы, или статины), производные фиброевой кислоты (фибраты),
никотиновая кислота и ее производные, а также секвестранты желчных кислот.
Различия в химическом строении и механизмах действия этих препаратов
обусловливают их воздействие на различные составляющие липидного спектра (табл.
3).
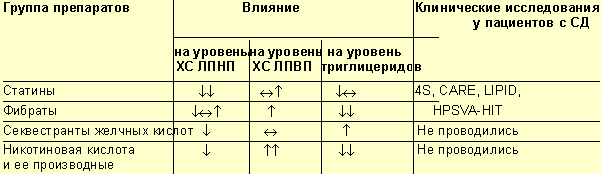
Группы гиполипидемических препаратов, применяемых для
лечения нарушений липидного обмена при СД 2 типа, и их влияние на липидный
спектр
В настоящее время в России доступны все шесть препаратов, представленных в
классе ингибиторов ГМГ-КоА-редуктазы: оригинальный розувастатин,
появившийся на рынке в 2004 г., а также оригинальные и дженерические
аторвастатин, симвастатин, правастатин, флувастатин и ловастатин.
Несмотря на разное химическое строение, все представители статинов обладают
одинаковым механизмом действия, который заключается в обратимом ингибировании
ГМГ-КоА-редуктазы — ключевого фермента синтеза холестерина de novo в клетках
печени. Уменьшение образования внутриклеточного холестерина ведет к активации на
поверхности гепатоцитов рецепторов к апобелкам В и Е, что приводит к увеличению
захвата ЛПНП, ЛПОНП, ЛПВП и уменьшению их содержания в крови. Таким образом,
терапия статинами ведет к выраженному снижению холестерина и ЛПНП, а также
умеренному снижению уровня триглицеридов [2]. Помимо влияния на липидный спектр,
описаны плеотропные антиатерогенные эффекты статинов: влияние на эндотелий
(сохранение/восстановление барьерной функции эндотелия; сосудорасширяющий эффект
за счет увеличения синтеза NO-синтазы), антитромботический эффект (снижение
агрегации тромбоцитов и увеличение фибринолиза), противовоспалительное действие,
уменьшение пролиферации гладкомышечных клеток, стабилизация липидного ядра и
фиброзной капсулы атеросклеротической бляшки [1].
Статины являются препаратами выбора для снижения уровня ХС ЛПНП, а также для
лечения комбинированной дислипидемии.
Эффективность статинов носит дозозависимый характер (табл. 4) [6]. Начальные
дозы препаратов, по сути являющиеся минимальными эффективными дозами, а также
режим и кратность дозирования приведены в таблице 5. Эквипотенциальные дозы
препаратов приведены в таблице 4. Поскольку в настоящее время известен эффект от
воздействия каждой дозы препарата на уровень ОХС и ХС ЛПНП, начинать терапию
целесообразно с того препарата, минимальная доза которого позволит сразу достичь
целевого показателя — это сократит количество визитов к врачу и позволит
повысить приверженность лечению. Максимальный эффект фиксированной дозы
препарата развивается через 4–8 нед, что следует учитывать при решении вопроса о
необходимости увеличения дозы. При достижении целевых значений ХС ЛПНП
рекомендуется исследование липидного спектра ежеквартально в течение первых 6
мес терапии и каждые 6–12 мес в дальнейшем. При выборе препарата необходимо
учитывать, что терапия назначается пожизненно, поэтому немаловажное значение
имеет стоимость лечения. Во-первых, в настоящее время доступны как оригинальные,
так и дженерические препараты, причем последние сопоставимы с первыми по
эффективности, но значительно уступают им в стоимости, и большинство
специалистов сходятся во мнении, что лучше назначить пациенту дженерический
препарат, чем не проводить лечения вообще. Во-вторых, назначение наиболее
эффективного в своем классе лекарственного средства в дозе, которая сразу же
позволит достичь целей лечения, позволит уменьшить затраты на повторные
исследования липидного спектра и визиты к врачу, необходимые для увеличения
дозы.
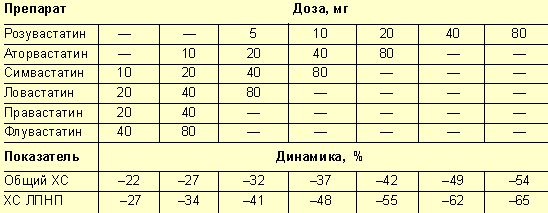
Сравнительная эффективность статинов [6]
Форма выпуска и режим дозирования статинов

Противопоказаниями к назначению статинов являются беременность и кормление
грудью, острое или хроническое заболевание печени в стадии обострения,
персистирующее повышение уровня трансаминаз (АЛТ, АСТ) — более чем в 3 раза выше
верхней границы нормы, злоупотребление алкоголем, патология мышц, исходный
уровень креатининфосфокиназы (КФК) более чем в 4 раза выше верхней границы
нормы.
Среди побочных эффектов наиболее часто встречаются гастроинтестинальные
нарушения (запоры, метеоризм, иногда тошнота, диспепсия), реже — нарушения со
стороны центральной нервной системы (головная боль, головокружение, бессонница),
слабость [6, 7, 9, 12–14]. В результате терапии статинами возможно развитие
миалгии, миозита/миопатии или рабдомиолиза (единичные случаи!). Вероятность
развития миалгии при приеме различных статинов не превышает 5%. Частота развития
миопатии/миозита обычно составляет 0,1–0,2% [2, 6, 9], это побочное явление
является показанием к снижению дозы или прекращению терапии. Возможно
неспецифическое повышение уровня КФК при отсутствии болевых ощущений в мышцах и
других жалоб, которое проходит самостоятельно и не требует прекращения терапии.
У 0,5–2% пациентов при назначении статинов в максимальных или близких к ним
дозах отмечается увеличение уровня АЛТ и/или АСТ [2]; при уменьшении дозы
препарата или прекращении его приема уровень трансаминаз возвращается к норме
[31].
Рекомендуется исследование уровня КФК через 4–6 нед после начала терапии, не
реже 1 раза в 3 мес в период подбора дозы, далее при фиксированной дозе
препарата, отсутствии клинической симптоматики и повышения уровня КФК в анамнезе
— 1 раз в 6 мес. Исследование уровня АЛТ и АСТ в период подбора дозы проводят не
реже 1 раза в мес, далее при фиксированной дозе 1 раз в 3 мес. При повышении
уровня трансаминаз — более чем в 3 раза выше верхней границы нормы —
целесообразно снижение дозы препарата.
Производные фиброевой кислоты (фибраты) включают препараты II и III
поколения: безафибрат, ципрофибрат, гемфиброзил, фенофибрат. Механизм действия
фибратов опосредован через стимуляцию активируемых пролифератором пероксисом
α-рецепторов клеточного ядра (PPAR-α). Активированные РРАR-α связывают ДНК на
промоутере генов-мишеней, что приводит к модулированию экспрессии генов ключевых
белков, участвующих в метаболизме липопротеинов [16, 29]. Фибраты снижают
уровень триглицеридов и ЛПОНП на 20–50% и повышают уровень ЛПВП на 10–20%. Также
фибраты снижают на 5–20% уровень ЛПНП, однако это происходит лишь при нормальных
или близких к таковым уровню триглицеридов и ЛПОНП. При этом фибраты меняют
качественный состав ЛПНП путем уменьшения соотношения мелких плотных частиц ЛПНП
и крупных частиц ЛПНП. Последние лучше распознаются апо-В/Е-рецепторами в
гепатоцитах и клетках периферических тканей. Катаболизм ЛПНП по этому механизму
считается менее атерогенным и способствует снижению коронарного риска [17, 21].
Кроме антиатерогенных эффектов, связанных с модификацией липидного профиля,
производные фиброевой кислоты обладают также плеотропными эффектами: влияние на
состояние системы гемостаза, на процессы воспаления, улучшение
эндотелийзависимой вазодилатации.
Учитывая влияние фибратов на показатели липидного профиля, можно утверждать,
что фибраты являются препаратами 1-го ряда при низком уровне ЛПВП и/или
повышенном уровне триглицеридов (табл. 4),
они также могут быть использованы в качестве препаратов 2-го ряда в сочетании со
статинами при комбинированной дислипидемии.
Фибраты назначаются сразу в полной терапевтической дозе, за исключением
комбинированной терапии со статинами или случаев, когда у пациента имеются
нарушения функции почек.
Режим дозирования фибратов следующий: гемфиброзил — 600 мг 2 раза в день;
фенофибрат микроионизированный в капсулах — 200 мг 1 раз в день, в таблетках —
160 мг 1 раз в день; ципрофибрат — 100 мг 1–2 раза в день; безафибрат
короткодействующий — 200 мг 3 раза в день, пролонгированный — 400 мг 1 раз в
день.
Терапия фибратами абсолютно противопоказана при тяжелой недостаточности
функции почек и печени, имеющейся желчнокаменной болезни, при беременности и
лактации [21, 25, 28]. Среди побочных эффектов необходимо отметить нарушения со
стороны желудочно-кишечного тракта (5%): тошнота, диарея, анорексия, чувство
тяжести в эпигастрии, метеоризм, боли в животе, также может иметь место
транзиторное увеличение уровня АЛТ, АСТ, КФК [18, 27, 30]. Приблизительно у 5%
больных наблюдаются головная боль, системное головокружение, слабость, нарушения
сна, тревога, у 2% пациентов возможно появление кожной аллергической сыпи [25,
27]. Другие побочные эффекты включают миалгию, миопатию/миозит и отдельные
случаи рабдомиолиза [28]. Миопатия/миозит развивается обычно в течение 2 мес
после начала терапии. Вероятность развития миозита возрастает при нарушении
функции почек или одновременном назначении статинов. Отмечены случаи
рабдомиолиза при комбинированной терапии ловастатином/гемфиброзилом и
церивастатином/гемфиброзилом, что обусловлено метаболизмом препаратов обоих
классов через систему цитохрома Р450 3А4 [29]. Через 6 нед после начала терапии
может иметь место повышение уровни креатинина и мочевины в сыворотке [22, 24],
после отмены фибратов функция почек у большинства пациентов возвращается к
исходной. Больным с уже имеющимся нарушением функции почек и пациентам,
перенесшим пересадку почки, фибраты следует назначать с большой осторожностью
[23]. При назначении фибратов необходимо контролировать уровень КФК, АЛТ и АСТ
так же, как при применении статинов.
Никотиновая кислота и ее производные являются наиболее эффективными
препаратами для повышения уровня ХС ЛПВП, они также снижают уровень
триглицеридов и ХС ЛПНП. Однако из-за отрицательного влияния на углеводный обмен
вследствие повышения инсулинорезистентности эти препараты не могут
использоваться в качестве терапии 1-го ряда у пациентов с СД 2 типа. Кроме того,
данные препараты ведут к усугублению гиперурикемии, а также могут провоцировать
обострение язвенной болезни и вызывать нарушение функции печени. С учетом
вышесказанного никотиновая кислота и ее производные используются в качестве
препаратов 2-го ряда у пациентов с высоким сердечно-сосудистым риском и доза
препарата обычно не превышает 1 г в сутки. Данные препараты могут использоваться
в комбинации со статинами или фибратами под контролем КФК, АЛТ, АСТ.
Секвестранты желчных кислот связываются с желчными кислотами в
просвете кишечника и препятствуют их обратному всасыванию, что приводит к
снижению ХС ЛПНП. Однако секвестранты желчных кислот повышают уровень
триглицеридов, в связи с чем не рекомендовано их использование при уровне
триглицеридов > 3 ммоль/л. Побочными эффектами являются высокая частота развития
гастроинтестинальных нарушений, а также нарушение всасывания других препаратов.
Секвестранты желчных кислот могут использоваться в качестве препаратов 2-го ряда
при повышении уровня ХС ЛПНП.
Выбор гиполипидемических препаратов в зависимости от
варианта дислипидемии при СД 2 типа

Одной из основных задач диабетологической службы является не только
вторичная, но и первичная профилактика ССЗ у пациентов с СД 2 типа, в частности
активное выявление и лечение нарушений липидного обмена. Изменение образа жизни
и модификация питания в сочетании с жестким контролем гликемии, несомненно,
могут оказать благоприятный эффект у определенной группы пациентов. Однако
большинству больных СД 2 типа для коррекции нарушений липидного обмена и
снижения сердечно-сосудистого риска требуется назначение медикаментозной
гиполипидемической терапии, основными представителями которой являются
ингибиторы ГМГ-КоА-редуктазы (статины) и производные фиброевой кислоты (фибраты).
Литература
- Аронов Д. М. Плеотропные эффекты статинов. Русский медицинский журнал. Т.
9. № 13-14.
- Шевченко О. П., Шевченко А. П. Статины - ингибиторы ГМГ-КоА-редуктазы. М.:
Реафарм, 2003.
- American Diabetes Association. Management of dyslipidemia in adults with
diabetes (position statement)//Diabetes. Саге. 2002, 25: 74-77.
- American Diabetes Association. Evidence-based nutrition principles and
recommendations for the treatment and prevention of diabetes and related
complication (position statement)//Diabetes. Саге. 2002; 25: 50-60.
- American Diabetes Association. Diabetes mellitus and exercise (position
statement)//Diabetes. Саге. 2001; 24: 51-55.
- Davidson М. Н. 11 Rosuvastatin: а highly efficacious statin for treatment
of dyslipidaemia//Expert. Opin. Investig. Drugs. 2002; 1: 125-141.
- Goldberg R. B., Mellies M. J., Sacks F. M. et al. Cardiovascular events
and their reduction with pravastatin in diabetic and glucose-intolerant
myocardial infarction survivors with average cholesterol levels: subgroup
analyses in the Cholesterol And Recurrent Events (CARE) Trial//Circulation.
1998; 98: 2513-2519.
- Haffner S. M., Alexander С. М., Cook T. J. et al. Reduced coronary events
in simvastatin-treated patients with coronary heart disease and diabetes or
impaired fasting glucose levels//Arch. Intern. Med. 1999; 159: 2661-2667.
- Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study
of cholesterol lowering with simvastatin 5963 people with diabetes: randomized
placebo-controlled trial//Lancet. 2003; 361: 2005-2016.
- Henry R. Preventing сardiovascular complications of type 2 diabetes: focus
on lipid management//Clinical. Diabetes. 2001: 19 (3).
- Kannel W. B., McGee D. L. Diabetes and glucose tolerance as risk factors
for cardiovascular disease: the Framingam Study//Diabetes. Care. 1979; 2:
120-126.
- Pyorala K., Pederson T. R., Kjekshus J. et al. Cholesterol lowering with
simvastatin improves prognosis in diabetic patients with coronary heart
disease: a subgroup analysis of the Scandinavian Simvastatin Survival Study
(4S)// Diabetes. Care. 1997; 20: 614-620.
- The Long-term Intervention of Pravastatin on Ischaemic Disease (LIPID)
Study Group. Prevenion of cardiovascular events and death with pravastatin in
patient with coronary heart disease and a broad range of initial cholesterol
levels// N. Engl. J. Med. 1998; 339: 1349-1357.
- Tuomilehto J. Interrupting the atherosclerotic process in diabetes: when
and how should we treat?//Advanced studies in medicine. 2002; 2 (22): 800-807.
- UK Prospective Diabetes Study (UKPDS) Group. Risk factors for coronary
artery disease in non-insulin dependent diabetes mellitus//Diabetes. Care.
2002; 25: 74-77.
- Tugwood O., Issemann I., Anderson R. G. et al. The mouse peroxisome
proliferator activated receptor recognizes a flanking sequence of the rat acyl
CoA oxidase gеnе//EMBO. 1992; 11: 433-439.
- Brown W. V., Dujovne С., Farquhar J. W. et al. Effects of fenofibrate on
plasma lipids. Double-blind, multicenter study in patients with type IIА or
IIВ hyperlipidemia//Arteriosclerosis. 1986; 6: 670-678.
- Farnier M., Bonnefous F., Debbas М. et al. Comparative efficacy and safety
of micronized fenofibrate and simvastatin in patients with primary type IIа or
IIЬ hyperlipidemia//Arch. Intern. Med. 1994; 154: 441-449.
- Munoz А., Guichard J. P., Reginault P. H. Micronized fenofibrate//Atherosclerosis
1999; 110: 45-54.
- Poulter H. The impact of micronized fenofibrate on lipid subfractions and
on reactung HDL-targets in 7,098 patients with dyslipidaemia//Вr. J. Cardiol.
1999; 6: 682-685.
- Kiortsis D. N. et al. Efficacy of combination of atorvastatin and
micronised fenofibrate in the treatment of severe mixed hyperlipidemia//Еur.
J. Clin. Pharmacol. 2000; 56: 631-635.
- Tsimichodimos V., Kakafika А., Elisaf М. Fibrate treatment can increase
serum creatinine levels//Nephrol. Dial. Transplant. 2001; 16: 1301.
- Broeders N., Кnоор С., Antoine M., Tielemans С. Fibrate-induced increase
in blood urea and creatinine: is gemfibrozil the only innocuous agent?//Nephrol.
Dial. Transplant. 2000; 15: 1993-1999.
- Tsimichodimos H., Bairaktari Е., Elisaf M. Fibrate-induced increase in
serum urea and creatinine levels//Nephrol. Dial. Transplant. 2002; 17: 682.
- Adkins J. C., Faulds D. Micronised fenofibrate: а review оf its
рharmacological properties and clinical efficacy in the management of
dyslipidemia//Drugs. 1997; 54: 615-633.
- Davignon P. Fibrates: а review of important issues and recent findings//Can.
J. Cardiol. 1994; 10 (Suppl В): 61-71.
- Shepherd J. Fibrates and statins in the treatment of hyperlipidaemia: an
appraisal of their efficacy and safety//Еur. Heart. J. 1995; 16: 5-13.
- Alexandridis O., Pappas G., Elisaf M. Rhabdomyolysis due to combination
therapy with cervistatin and gemfibrozil//Am. J. Med. 2000; 109: 261-262.
- Schoonjans К., Martin G., Staels В. et аl. Peroxisome
prolferator-activated receptors, orphans with ligands and functions//Сurr.
Opin. Lipidol. 1997: 8: 159-166.
- Kirchgassler K. J., Schmitz Н. et al. Effectiveness and tolerability of
12-week treatment with micronized fenofibrate200 in а drug-monitoring
programme involving 9884 patients with dyslipidaemia//Clin. Drug. Invest.
1998; 15: 197-204.
- Hsu I., Spinier S. A. et al. Comparative evaluation of the safety and
efficacy of НМG-СоА-reductase inhibitors monotherapy in the treatment of
primary hypercholesterolemia//Ann. Pharmacol. 1995; 29: 743-759.
- National Diabetes Education Program. Control the ABCs of Diabetes, 2002.
Статья опубликована в журнале
Лечащий Врач

