Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Гликемический контроль при лечении артериальной гипертонии у
больных с метаболическим синдромом
В. И. Маколкин, член-корреспондент РАМН, доктор медицинских наук,
профессор
Ф. Н. Зябрев
ММА им. И. М. Сеченова, Москва
Артериальная гипертензия (АГ) остается в настоящее время одним из наиболее
распространенных заболеваний. В связи с поиском оптимальных методов лечения
появились новые исследования, которые показали, что для достижения целевых
значений артериального давления (АД) монотерапии, как правило, недостаточно и
требуется комбинация антигипертензивных препаратов. Кроме того, АГ часто
сочетается с другими факторами риска, различными синдромами (метаболический
синдром, дислипидемия, гиперурикемия) и заболеваниями (сахарный диабет,
ишемическая болезнь сердца, цереброваскулярная патология и др.), которые
ухудшают прогноз и требуют от врача иного подхода к терапии. При выборе
антигипертензивной терапии должны учитываться и другие эффекты от лечения [1–4].
Поиск наилучшей комбинации для лечения больных АГ с метаболическим синдромом
определил появление исследования STAR (Study of Trandolapril-verapamil and
Insulin Resistance). Предпосылкой его явился анализ клинических исследований,
показавший способность ингибиторов ангиотензинпревращающего фермента (иАПФ) и
блокаторов (антагонистов) рецепторов к ангиотензину II (АРА II) снижать риск
развития сахарного диабета [5–7]. Оставалось неясным, можно ли нейтрализовать
побочное действие тиазидных диуретиков у больных с нарушенной толерантностью к
глюкозе (НТГ) и метаболическим синдромом путем добавления к терапии блокаторов
АРА II — лозартана. Как известно, недигидропиридиновый блокатор кальциевых
каналов верапамил длительного действия уменьшает частоту развития
сердечно-сосудистых осложнений в той же степени, что и тиазидный диуретик, но
обладает при этом метаболической нейтральностью. Это позволяет предположить, что
при снижении АД комбинацией иАПФ — трандолаприла и верапамила длительного
действия (Т+В) — можно добиться лучшего эффекта в терапии больных с НТГ и
метаболическим синдромом, нежели при использовании комбинации лозартана и
гидрохлортиазида (Л+Г). Таким образом, целью исследования STAR явилось сравнение
воздействия на больных АГ с метаболическим синдромом комбинации иАПФ +
недигидропиридиновый антагонист кальциевых каналов с комбинацией АРА II +
тиазидный диуретик. Исследование проводилось под контролем уровня гликемии.
STAR — открытое проспективное рандомизированное мультицентровое исследование
со слепой оценкой результатов.
На начальном этапе, во время которого гипотензивная терапия отменялась, при
диастолическом артериальном давлении (ДАД) ≥ 100 мм рт. ст. либо при
систолическом артериальном давлении (САД) ≥ 160 мм рт. ст. назначался клофелин
до 1,5 таблетки (0,075 мг) дважды в день. После этого этапа составлялась
характеристика пациентов и проводилась рандомизация (с помощью программы Web
Rando) на две группы:
- в 1-й группе больные получали 2/180 мг трандолаприла/верапамила
пролонгированного действия (Т+В);
- во 2-й группе пациенты получали 50/12,5 мг лозартана/гидрохлортиазида (Л+Г).
Если через 4 нед после начала лечения не удавалось достичь целевого значения
АД (САД < 130 мм рт. ст.), то дозу в комбинации Т+В увеличивали до 4/240 мг, а в
комбинации Л+Г — до 100/25 мг (однократно в сутки). Если целевой уровень САД все
же не был достигнут, то к терапии добавляли клофелин в обеих группах.
Запланированная продолжительность исследования составляла 52 нед. Первые 12 нед
больной посещал врача каждые 2 нед, в дальнейшем — каждые 4 мес. Во время
каждого визита у больных контролировали основные показатели метаболизма,
приверженность к лечению (на основе подсчета количества использованных таблеток)
и побочные эффекты. Пероральный глюкозотолерантный тест (ГТТ) и другие
лабораторные диагностические процедуры проводились в начале исследования, далее
— на 12-й и 52-й неделе (либо при последнем визите).
Критериями включения в исследование являлись: возраст старше 21 года и
диагностированный метаболический синдром (уровень глюкозы натощак от 100 до 125
мг/дл; наличие контролируемой гипертонии (САД < 140 мм рт. ст.) при терапии
двумя антигипертензивными препаратами, либо САД при монотерапии от 130 до 160 мм
рт. ст.; наличие одного из перечисленных ниже факторов: липопротеиды высокой
плотности (ЛПВП) < 40 мг/дл у мужчин, < 50 мг/дл у женщин; общий холестерин >
150 мг/дл; объем талии более 102 см у мужчин, более 89 см у женщин).
Из исследования исключались: пациенты с сахарным диабетом, принимающие более
двух антигипертензивных препаратов; пациенты со вторичной АГ; пациенты,
принимающие нестероидные противовоспалительные препараты (НПВП), ингибиторы
циклооксигеназы-2, ниацин в дозе > 100 мг/сут, либо петлевые диуретики; пациенты
с почечной недостаточностью (креатинин сыворотки > 1,4 мг/дл и/или отношение
альбумин/креатинин в моче > 0,3).
Первичной конечной точкой исследования являлось изменение степени
толерантности к глюкозе (ГТТ в начале исследования и в его конце — на 52-й
неделе, регистрировался уровень глюкозы крови и уровень инсулина).
Вторичными конечными точками исследования являлись изменения уровня АД, ЧСС;
уровня глюкозы натощак и при проведении ГТТ; развитие новых случаев сахарного
диабета (уровень глюкозы крови натощак ≥ 126 мг/дл либо уровень глюкозы крови
через 2 ч после сахарной нагрузки ≥ 200 мг/дл); площадь под кривой глюкозы от 0
до 120-й минуты; ожидаемая чувствительность к инсулину [9–10]; гликозилированный
гемоглобин — HbA1c; липидный профиль; степень достижения целевого АД.
Регистрировались возможные побочные явления.
Результаты
Из принявших участие в исследовании 240 амбулаторных больных, которые
случайным образом были распределены в группу терапии Т+В либо Л+Г, завершили
52-недельное исследование 77,5%. Преждевременный выход из исследования было
одинаков в обеих группах — 24 пациента в 1-й группе (Т+В), 23 пациента во 2-й
группе (Л+Г): причиной послужили серьезные побочные эффекты. 7 больных выбыло по
немедицинским причинам. Обе группы были равными по демографическим
характеристикам.
Средний возраст больных составлял 57,7 ± 10,3 года в 1-й группе (Т+В) и 55,4
± 9,7 года во 2-й группе (Л+Г), из которых женщины составляли 53,8 и 48,8%
соответственно.
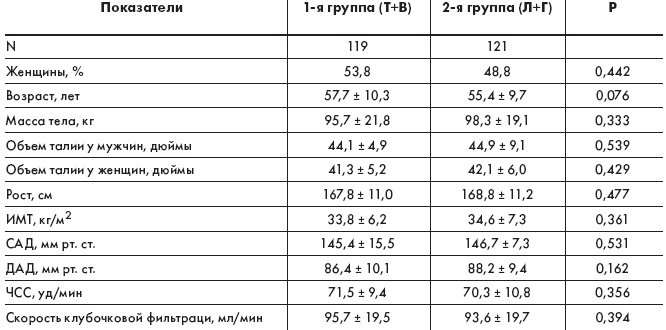
Характеристика больных в начале исследования
Были обобщены данные анализов 108 больных из 119 (91%) из 1-й группы (Т+В) и
107 больных из 121 (88%) 2-й группы (Л+Г). Средняя продолжительность лечения
составляла 46,9 ± 13,5 нед.
Измерение уровня глюкозы. Уровень глюкозы при ГТТ увеличился
во 2-й группе (Л+Г) и остался на прежнем уровне в 1-й группе (Т+В). Разница
между двумя группами составляла 1,0 ± 0,3 ммоль/л (р < 0,001) на 12-й неделе и
1,6 ± 0,5 ммоль/л (р < 0,001) на 52-й нед.
Сравнение уровня глюкозы натощак выявило разницу между двумя группами не
только на 12-й неделе, но и к концу исследования. Во 2-й группе (Л+Г) сахарный
диабет к 12-й неделе развивался почти в 3 раза чаще, чем в 1-й группе (Т+В): 20
пациентов из 93 во 2-й группе (Л+Г) (21,5%) против 6 пациентов из 86 (7%) в 1-й
группе (Т+В) (р = 0,007). Подобные результаты были и к концу исследования: в 1-й
группе (Т+В) — 10 пациентов из 91 (11%), во 2-й группе (Л+Г) — 25 из 94 (26,6%)
(р = 0,002). К концу исследования уровень инсулина оказался более высоким в
группе больных, получавших комбинацию Л+Г.
Средний уровень HbA1c был выше во 2-й группе (Л+Г) в период всего наблюдения.
Более того, доля пациентов, у которых HbA1c был выше 7% к концу исследования,
оказалась выше во 2-й группе (Л+Г): 2,6% в 1-й группе (Т+В) против 9,6% во 2-й
группе (Л+Г) (р = 0,05).
Наконец, анализ ГТТ в подгруппах больных, получавших низкие начальные дозы
препаратов, выявил снижение гликемии в 1-й группе (Т+В): -1,04 ± 1,99 ммоль/л и
повышение гликемии во 2-й группе (Л+Г): 0,61 ± 2,40 ммоль/л. Разница была более
заметной в подгруппе пациентов, получавших высокие дозы препаратов: -0,01 ± 2,67
ммоль/л в 1-й группе (Т+В) против +1,65 ± 4,56 ммоль/л во 2-й группе (Л+Г).
Артериальное давление. На момент окончания исследования не
было обнаружено значимой разницы в величинах САД по обеим группам (130,6 ± 15,7
и 128,8 ± 14,0 мм рт. ст. в 1-й и 2-й группах, р = 0,179), в величинах ДАД (78,7
± 10,0 и 78,8 ± 8,8 мм рт. ст. соответственно, р = 0,605), а также в показателях
ЧСС (71,9 ± 10,0 и 72,1 ± 11,2 уд/мин соответственно, р = 0,457). На 12-й и 26-й
нед наблюдалась разница между двумя группами в количестве больных, достигших
целевого АД < 130 мм рт. ст.: к 12-й нед 58,9% во 2-й группе (Л+Г) и 47,3% в 1-й
группе (Т+В) (р = 0,047), а к 26-й неделе 59,0% в группе Л+Г и 46,0% в группе
Т+В (p = 0,009). К окончанию исследования такой разницы не наблюдалось: 49,6% в
1-й группе (Т+В) и 60,8% во 2-й группе (Л+Г), (р = 0,06).
Липиды и маркеры воспаления. Не было обнаружено разницы
между группами по показателям общего холестерина (р = 0,20), триглицеридов (р =
0,36), ЛПНП (р = 0,24), ЛПВП (р = 0,13), С-реактивного белка (в группе Т+В 5,9 ±
6,1 в начале и 6,6 ± 7,6 мг/л в конце исследования, в 1-й группе (Л+Г) 5,3 ± 4,6
в начале и 6,0 ± 6,0 мг/л в конце исследования; р = 0,76).
Побочные явления. Частота развития побочных эффектов (5% и
более) в каждой подгруппе была одинакова. Следует отметить, что кашель (6%
против 1%, р = 0,035) и боль в конечностях (5% против 0%, р = 0,014) развивались
в группе больных, получавших комбинацию Т+В. Количество серьезных побочных
эффектов было равным в обеих группах (6 больных из 119 — 5%) и 7 больных из 121
— 6% в 1-й и 2-й группах соответственно). На фоне терапии летальность не
зарегистрирована ни в одной из групп больных. Изменения уровня калия сыворотки
(в начале исследования 4,2 ± 0,4 ммоль/л) к концу исследования были значимы
статистически, но не клинически (в конце исследования +0,01 ± 0,38 против -0,17
± 0,40 ммоль/л в 1-й и 2-й группах соответственно, р < 0,001). Не обнаружено
связи уровня калия сыворотки с уровнем инсулина или глюкозы. Также не было
значимого изменения массы тела (-0,2 ± 5,2 против -0,5 ± 4,4 кг в 1-й и 2-й
группах соответственно), изменения скорости клубочковой фильтрации (-10,5 ± 15,5
против -9,0 ± 15,2 мл/мин соответственно).
Исследование STAR показывает, что у больных с метаболическим синдромом и НТГ
предпочтительнее использовать фиксированную комбинацию иАПФ и
недигидропиридинового блокатора кальциевых каналов, так как это позволяет
избежать ухудшения результатов ГТТ (в отличие от комбинации блокатор РА II +
тиазидный диуретик), хотя обе комбинации одинаково эффективны в плане достижения
целевого уровня АД.
Во 2-й группе (Л+Г) ухудшение результатов ГТТ сопровождалось повышением
показателя количества HbA1c и увеличением уровня глюкозы натощак к концу
исследования; к тому же увеличивался уровень инсулина крови. Разница по двум
группам в количестве инсулина и нарушении обмена глюкозы наблюдалась уже на 12-й
неделе терапии. В настоящее время это первое многоцентровое исследование, где
изучались изменения в результатах ГТТ при разных комбинированных схемах лечения
(иАПФ + антагонист кальциевых каналов и АРА-II + тиазидный диуретик) у больных с
метаболическим синдромом и НТГ [11]. К тому же оказалось, что тиазиды у больных
с НТГ или метаболическим синдромом приводят к увеличению уровня гликемии даже
при использовании их в низких дозах, и комбинация их в сочетании с высокой дозой
лозартана не меняет ситуацию [11–14].
Известно, что при использовании тиазидов часто развивается сахарный диабет
[5–7, 12–17]. В исследовании STAR разница в уровне гликемии натощак выявлялась
уже на 12-й неделе с тенденцией к дальнейшему значительному увеличению к
окончанию исследования. Во 2-й группе (Л+Г) к концу исследования было выявлено
больше больных с увеличенным уровнем HbA1c, инсулина, гликемии при ГТТ.
Высказывалось предположение, что сопутствующее использование блокаторов
ренин-ангиотензин-альдостероновой системы (РААС) может защитить больного от
нарушения обмена глюкозы [18–20]. В исследовании STAR впервые показано, что
тиазидный диуретик приводит к нарушению обмена глюкозы в присутствии блокатора
РААС [11].
Комбинация блокатора РААС с тиазидным диуретиком часто назначается больным с
АГ и метаболическим синдромом для снижения АД [8, 21]. Исследование STAR
показало, что использование комбинации Л+Г позволяет намного большему количеству
больных достигнуть целевого АД к 12-й и 26-й неделе по сравнению с больными,
принимающими комбинацию Т+В, но это преимущество отсутствует на 52-й неделе или
на момент окончания исследования. Важно отметить, что наибольшее ухудшение
обмена глюкозы во 2-й группе (Л+Г) наблюдалось в эти же сроки (12-я и 26-я
неделя). Остается неясным, может ли лучший контроль АД при помощи блокатора РААС
и тиазидного диуретика вызвать инсулинорезистентность или НТГ. Более того, этот
эффект не связан с ранним назначением высокой дозы тиазидного диуретика.
Следовательно, ухудшение гликемического контроля в группе высокого риска
развития сахарного диабета является опасным, вызывает новые случаи развития
диабета и повышает сердечно-сосудистый риск [22, 23].
Чтобы лучше понять механизм развития сахарного диабета, исследование было
продлено еще на 6 мес. Всем больным назначили комбинацию Т+В. Первичная цель —
изучить результаты ГТТ через 6 мес.
В заключение следует сказать, что только в США АГ встречается почти у каждого
четвертого взрослого [24]. Хорошо известен угрожающий прогноз по ожидаемому
увеличению частоты случаев сахарного диабета — к 2020 г. в мире больных сахарным
диабетом будет около 300 млн [25]. Примерно у 85% больных этим заболеванием
встречается АГ, и это сочетание усугубляет течение каждого из них. К тому же АГ
при сахарном диабете имеет свои особенности в виде очень частого и быстрого
развития поражений органов-мишеней (микроальбуминурии, ретинопатии, нефропатии,
гипертрофии левого желудочка, нарушения функции сердца, эндотелиальной
дисфункции, снижения эластичности и повышения «жесткости» сосудов).
Использование комбинации иАПФ трандолаприла и антагониста кальция
пролонгированного действия у больных с НТГ, неизмененной функцией почек и
метаболическим синдромом минимизирует риск развития сахарного диабета за 1 год,
чего не наблюдается при использовании комбинации тиазидного диуретика
гидрохлортиазида и блокатора рецепторов к ангиотензину II лозартана. Необходимы
дальнейшие исследования, которые бы окончательно решили вопрос о возможном «диабетогенном»
действии различных доз гидрохлортиазида, с одной стороны, а с другой — выяснили
бы, какие дозы блокаторов АРА II, а также иАПФ могли бы «компенсировать» это
диабетогенное действие гидрохлортиазида.
Статья опубликована в журнале
Лечащий Врач

