Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Ингибиторы протонной помпы как
основа лечения кислотозависимых заболеваний
И.В. Маев, Д.Н. Андреев, А.Ю. Гончаренко,
Д.Т. Дичева
Кафедра пропедевтики внутренних болезней и
гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И. Евдокимова
Минздрава РФ
История изучения физиологической роли желудочного
кислотообразования насчитывает несколько столетий. В
начале XVI в. знаменитый алхимик Парацельс
предположил наличие в желудке кислоты. Спустя
столетия в 1823 г. английский врач и химик Уильям
Праут доказал наличие соляной кислоты в желудочном
соке. Позже роль желудочного кислотообразования
изучалась российскими физиологами И.П. Павловым и
А.М. Уголевым. Однако одно из самых значимых
открытий совершил в 1893 г. Камилло Гольджи.
Итальянский гистолог и патолог установил, что
соляную кислоту вырабатывают париетальные клетки,
располагающиеся в наружной части фундальных
(главных) желез желудка. Уже на этапе современного
развития медицины именно эти клетки рассматриваются
как одна из важнейших терапевтических мишеней.
Суммарное количество париетальных клеток в
желудке у здорового человека приближается к одному
миллиарду (1000×106). Париетальная клетка
имеет овальную или пирамидальную форму.
Отличительными особенностями этой клетки является
крупный размер, большое количество митохондрий,
секреторные канальцы и тубуловезикулы. Механизм
секреции соляной кислоты париетальными клетками
обусловлен наличием специфического трансмембранного
переносчика ионов водорода – Н+/К+-АТФазы, также
известной как протонная помпа.
Протонная помпа относится к семейству белков –
АТФаз P-типа, отвечающих за транспорт ионов через
клеточные мембраны. Этот белок транспортирует ион Н+
через апикальную мембрану из цитозоли париетальной
клетки в просвет секреторного канальца в обмен на
ион К+. Источником энергии для данного транспорта
является гидролиз молекулы АТФ. Последующий выход
ионов К+ из цитозоли сопряжен с выходом ионов Cl- по
типу симпорта. В итоге в просвете канальцев
происходит взаимодействие ионов H+ и Cl- с
образованием соляной кислоты (рис. 1).
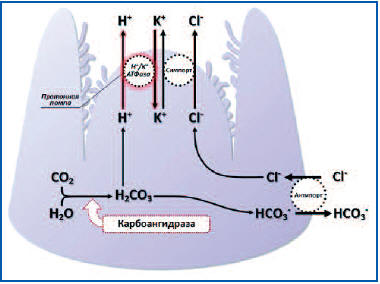
Рис. 1. Секреция соляной кислоты париетальной
клеткой желудка. Основные транспортные системы, роль
H+/K+-АТФазы
Примечание. В секреции задействованы Н+/К+-АТФаза
(протонная помпа), переносчик ионов K+/Cl- по типу
симпорта, переносчик ионов НСО3-/Cl- по типу
антипорта и фермент карбоангидраза, обеспечивающий
синтез Н СО из углекислого газа и воды.
Фундаментальные исследования отечественных и
зарубежных ученых позволили установить, что функции
соляной кислоты желудка многообразны:
- создание кислой среды, необходимой для
воздействия ферментов желудочного сока;
- активация пепсиногенов и трансформация их в
пепсины;
- денатурация белков в полости желудка;
- влияние на моторную активность желудка, в
частности его выходного отдела;
- формирование «кислотного» антибактериального
барьера на уровне желудка;
- стимуляция панкреатической секреции.
Однако сегодня мы знаем, что соляная кислота
играет не только важную роль в процессах
пищеварения, но и при ее избыточной продукции
является сильным фактором агрессии, истощая
возможности кислотопротекции различных структур
желудочно-кишечного тракта. Причины повышенной
секреции соляной кислоты разнообразны и могут быть
обусловлены генетически детерминированным
увеличением массы париетальных клеток, повышенным
высвобождением гастрина в ответ на прием пищи, а
также нарушением нейроэндокринной регуляции
кислотообразования (усиление вагусного влияния,
гиперплазия и гиперфункция G-клеток и ECL-клеток).
Таким образом, уровень внутрижелудочной
кислотности у конкретного пациента определяется
числом функционирующих париетальных клеток и
возможностями нейтрализации соляной кислоты
щелочными компонентами желудочного сока. В данном
контексте важную роль играет скорость
кислотопродукции – чем выше этот показатель, тем
меньше вероятность нейтрализации и, соответственно,
выше кислотность желудочного сока. Именно избыточное
кислотообразование лежит в основе патогенеза
состояний, объединенных в XX в. термином «кислотозависимые
заболевания» (КЗЗ).
По современным представлениям КЗЗ – это группа
нозологических единиц, ассоциируемых с кислотной
агрессией желудочного сока. Причинами КЗЗ может
явиться дисбаланс между механизмами кислотопродукции
и кислотонейтрализации, недостаточность кардиального
или пилорического сфинктеров, иррациональное питание
и злоупотребление алкоголем.
Спектр патологических состояний, которые включает
в себя термин КЗЗ, довольно широк:
- гастроэзофагеальная рефлюксная болезнь;
- функциональная диспепсия;
- хронический гастрит;
- хронический гастродуоденит;
- язвенная болезнь желудка/двенадцатиперстной
кишки (ДПК);
- эрозивно-язвенные поражения желудка и ДПК на
фоне приема нестероидных противовоспалительных
препаратов;
- эрозивно-язвенные поражения желудка и ДПК,
ассоциированные с гиперпаратиреозом;
- синдром Золлингера–Эллисона;
- хронический панкреатит.
Характерное хроническое течение КЗЗ, затяжные
обострения, разнообразие клинических проявлений
обусловливают частую обращаемость больных за
медицинской помощью. При этом стоит подчеркнуть, что
КЗЗ существенно снижают качество жизни больного и
оказывают значимый социально-экономический ущерб
примерно в той же мере, как и сердечнососудистые и
онкологические заболевания.
Несмотря на гетерогенность этиологических
процессов КЗЗ, их объединяет общий
патофизиологический фактор, ассоциируемый с
кислотно-пептической агрессией желудочного сока.
Общность этого патофизиологического звена определила
единую терапевтическую мишень – блокаду продукции
соляной кислоты париетальными клетками желудка.
Эпоха лечения КЗЗ насчитывает несколько этапов,
связанных с применением различных групп
фармакологических препаратов. С целью лечения этой
группы патологий использовались неселективные и
селективные М-холинолитики, блокаторы гистаминовых
H2-рецепторов, а также блокаторы гастриновых
CCK2-рецепторов. Однако введение в клиническую
практику ингибиторов протонной помпы (ИПП) привело к
революционному прорыву в лечении КЗЗ. С появлением
ИПП другие классы антисекреторных препаратов стали
постепенно вытесняться из клинической практики в
связи со значительно менее выраженным
антисекреторным эффектом и большим спектром побочных
действий. Сегодня можно без сомнения сказать, что
ИПП занимают передовое место в структуре
антисекреторных препаратов и являются «золотым
стандартом» в терапии КЗЗ.
В 1988 г. в Европе был зарегистрирован первый ИПП
– омепразол под торговым названием Лосек® (AstraZeneca,
Швеция). Уже в 1996 г. Лосек® стал самым продаваемым
фармацевтическим товаром в мире. При этом, несмотря
на более 20-летнюю историю, он до сегодняшнего дня
остается одним из наиболее востребованных
лекарственных средств.
Уникальность и клиническая эффективность ИПП
заключается в их высокоселективном механизме
действия. Данный класс препаратов необратимо
блокирует активные протонные помпы, встроенные в
апикальный полюс мембраны париетальных клеток. По
химической природе ИПП являются слабыми основаниями,
они накапливаются в канальцах париетальных клеток,
где в кислой среде происходит их протонирование и
преобразование в активную форму (сульфенамид).
Сульфенамид ковалентно с помощью дисульфидных связей
связывается с цистеиновыми группами протонной помпы,
что приводит к ингибированию фермента и угнетению
секреции соляной кислоты (рис. 2).

Рис. 2. Механизм действия ИПП
Кислотосупрессивный эффект ИПП по отношению как к
базальной, так и стимулированной секреции длится в
течение 24 ч и более. Примерно столько времени
требуется париетальной клетке на синтез и интеграцию
в мембрану новых молекул протонной помпы. Показано,
что однократный прием ИПП в средней терапевтической
дозе приводит к угнетению желудочной
кислотопродукции на 80–98%, что существенно больше
по сравнению с блокаторами гистаминовых
Н2-рецепторов (рис. 3). На сегодняшний день в
клиническую практику были внедрены и многие другие
представители ИПП, однако эталонным препаратом из
этой группы можно назвать эзомепразол (Нексиум®;
AstraZeneca, Швеция), который является
S-энантиомером омепразола. Именно детерминированная
пространственная ориентация определяет ряд
преимуществ эзомепразола по отношению к другим
представителям группы ИПП, являющимся рацематами
(смесь S- и R-изомеров). В рамках феномена
стереоселективности метаболизм эзомепразола как
S-изомера протекает в 3 раза медленнее, чем
метаболизм его рацемата (омепразола). Данное явление
находит свое отражение в увеличении такого
показателя, как площадь под кривой «концентрация в
плазме–время» (AUC). Следствием этого является
высокая биодоступность эзомепразола, что определяет
большее количество изомеров в кровотоке, которое
достигнет париетальных клеток. Преимущества
фармакокинетического профиля эзомепразола, позволяют
ему более эффективно и стабильно блокировать
протонную помпу. Отражением этого является тот факт,
что эзомепразол в 1,4 раза больше подавляет
базальный уровень желудочной секреции, чем омепразол
(90,7% против 64,5%).

Рис. 3. Сравнение суточной антисекреторной
активности блокаторов H2-рецепторов (ранитидин) и
омепразола
Тем не менее омепразол до сих пор является широко
назначаемым препаратом как в мире, так и в России.
Более того, в России до 90% от всех реализованных
ИПП составляет этот препарат. В целом этот тренд во
многом объясняется ценовой доступностью
многочисленных генериков омепразола.
К сожалению, стоит отметить, что в нашей стране
нет единого реестра, в котором бы сравнивалась
эффективность оригинального препарата и его
генериков. Как известно, не всегда генерик обладает
должной биологической, фармацевтической и
терапевтической эквивалентностью с оригинальным
препаратом – в силу использования некачественных
субстанций и вспомогательных веществ, а также малой
доступностью для контроля в сфере фармацевтической
продукции ряда стран-производителей (Индия, Китай,
Пакистан и др.). В связи с этим в настоящее время
практикующий врач нередко сталкивается с проблемой
недостаточной эффективности генерических препаратов.
Как уже было сказано выше, существенным доводом в
пользу назначения генериков всегда была их меньшая
стоимость по сравнению с оригинальным препаратом.
Однако с 2013 г. это преимущество было нивелировано
компанией AstraZeneca за счет существенного снижения
цены на оригинальный препарат омепразола – Лосек®.
Обращает на себя внимание тот факт, что данный
препарат выпускается в форме высокотехнологичной
таблетки МАПС (MUPS – Multiple Unit Pellet System).
Эта лекарственная форма омепразола запатентована
компанией AstraZeneca как самостоятельная ввиду ряда
структурных особенностей. Каждая МАПС-таблетка
состоит из множества микрогранул омепразола (∼1000),
покрытых дополнительной энтеросолюбильной защитной
оболочкой (рис. 4). В силу данной структуры
активно-действующее вещество не подвергается
агрессивному воздействию соляной кислоты, и
омепразол высвобождается лишь в щелочной среде ДПК,
что обеспечивает предсказуемый и воспроизводимый
антисекреторный эффект.

Рис. 4. Структура МАПС-таблетки препарата
Лосек® МАПС
Приведенные выше данные согласуются и с нашим
клиническим опытом, позволяющим свидетельствовать о
высокой эффективности Лосек® МАПС в терапии КЗЗ.
Таким образом, широкое распространение КЗЗ в
популяции обусловливает высокую востребованность ИПП
в ежедневной клинической практике. Оригинальный
препарат омепразола – Лосек® можно считать главой
семейства омепразолов. Лекарственная форма Лосек®
МАПС обеспечивает надежный антисекреторный эффект в
силу содержания множества кислотоустойчивых
микрогранул омепразола, опосредуя высвобождение
активного вещества лишь в щелочной среде ДПК.
Снижение стоимости Лосека МАПС в нынешнем году,
безусловно, обеспечивает большую доступность
оригинального высококачественного препарата для
пациентов.
Статья опубликована на сайте
http://www.gastroscan.ru

