Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Генитальная папилломавирусная инфекция (ПВИ) является одной из самых частых
инфекций, передаваемых половым путем (ИППП). Только в США ею поражено около 20
млн и ежегодно заражается 5,5 млн человек [16]. Чрезвычайная опасность и
важная социальная значимость этой инфекции обусловлена ее этиологической ролью
в развитии практически всех случаев рака шейки матки, около 50% других раков
аногенитальной области, а также целого ряда разновидностей злокачественных
новообразований верхних дыхательных путей и кожи [18, 23].
В России, где официально регистрируются лишь случаи аногенитальных
(венерических) бородавок, интенсивный показатель заболеваемости ими,
составивший в 2004–2005 гг. 32,9–32,1 случая на 100 тысяч населения,
свидетельствует об эпидемическом характере распространенности этой категории
ПВИ [5]. В то же время, даже с учетом 10-кратного роста регистрируемой за
последние 10 лет заболеваемости ПВИ [7], эти цифры не отражают масштабов ее
истинной распространенности. Во многом это связано со сложностью диагностики
субклинических и латентных форм инфекции.
При половом заражении вирус папилломы человека (ВПЧ) чаще всего приводит к
развитию аногенитальных бородавок, классической формой которых являются
остроконечные кондиломы — доброкачественные мягкие папилломатозные
разрастания, расположенные, как правило, в аногенитальной области и обычно
обусловленные ВПЧ 6 и 11 и реже другими, в том числе высокоонкогенными, типами
ВПЧ. В целом же не менее 35 типов ВПЧ (16, 18 и др.) вызывают дисплазию и рак
половых органов (шейки матки, вульвы, влагалища, полового члена), гортани и
заднего прохода [3].
Пик частоты ВПЧ-инфекции гениталий приходится на 18–25 лет — возраст
наивысшей половой активности. После 30 лет ее распространенность снижается, но
существенно возрастает частота дисплазий и рака шейки матки, причем пик
частоты последнего приходится на 45 лет.
К числу важных в эпидемиологическом и клиническом отношении особенностей
ПВИ-инфекции, наряду с ее нередким субклиническим течением, относится
длительность инкубационного периода (от нескольких месяцев до нескольких лет),
что также существенно затрудняет ее диагностику и лечение [11].
ВПЧ относятся к подгруппе А семейства паповавирусов (Papovaviridae).
Вирионы не имеют оболочки, диаметр их равен 50–55 нм. Геном представлен
двуспиральной кольцевидно скрученной ДНК, включает около 8000 основных пар и
кодирует всего 8 открытых рамок считывания. В процессе репликационного цикла
геном вируса экспрессирует от 8 до 10 белковых продуктов. Ранние белки (early),
контролирующие репликацию вируса, транскрипцию и клеточную трансформацию,
кодируются онкопротеинами Е6 и Е7. Поздние белки (late) L1 и L2 кодируют
структурные белки вириона. Белок L1 формирует капсомеры. Белки Е1 и Е2
регулируют репликацию вирусной ДНК и экспрессию генов. Онкогены Е6 и Е7 всегда
выявляются в опухолевых клетках, зараженных ВПЧ, в то время как другие
фрагменты вирусного генома могут быть утеряны в процессе его длительной
персистенции.
В инфицированных эпителиальных клетках на начальных стадиях вирусный
генетический материал персистирует в эписомальной форме, при этом клетка
способна продуцировать вирусные частицы. На более поздних стадиях геном вируса
интегрирует в клеточный геном, и способность к репродукции вируса
утрачивается. Интеграция вирусной ДНК в клеточную может индуцировать несколько
важных событий. Во-первых, она часто сопровождается потерей вирусного
материала, при этом обязательно обеспечивается сохранение генов Е6 и Е7;
во-вторых, независимо от делеций вирусный геном в интегрированной форме не
способен к полной репликации; в-третьих, индуцируется нестабильность
клеточного генома. Так, показано, что в канцерогенез шейки матки вовлечены
определенные участки хромосом, что указывает на множественность генетических
нарушений в опухолевой клетке. При интеграции вирусного генома в клеточный не
только сохраняется транскрипция вирусных генов, прежде всего Е6 и Е7, но и
активируется транскрипция некоторых клеточных генов.
Обнаружениe существенных различий в спектре синтезируемых этой опухолью РНК
указывает на разнообразие генетических механизмов, вовлеченных в процесс
канцерогенеза, обусловленного ВПЧ. В частности, белки Е6 и Е7 могут
инактивировать белки-супрессоры опухолевого роста р53 и рRb105 соответственно.
Кроме того, указанные онкобелки влияют на некоторые белки-циклины и
циклин-зависимые киназы, являющиеся регуляторами цикла деления клетки [15,
22].
В настоящее время доказано, что ВПЧ является онкогенным вирусом, связанным
не только с цервикальными и аногенитальными раками, но и с плоскоклеточным
раком гортани, предстательной железы, кожи [1] и др. (особенно на фоне
иммуносупрессии).
Чаще всего в ткани генитальных опухолей обнаруживаются ВПЧ 6, 11, 16, 18,
31, 33, 35, 41, 42, причем у одного больного может быть несколько типов ВПЧ
одновременно. ВПЧ инфицирует пролиферирующие эпителиальные клетки базального
слоя эпителия через механические, бактериальные и другие микроповреждения.
Репликация ДНК ВПЧ происходит только в клетках базального слоя, поэтому
методы лечения, направленные на удаление поверхностного слоя эпидермиса,
неэффективны и сопровождаются рецидивом заболевания. Инфицированные клетки
базального слоя служат постоянным источником инфицирования эпителиальных
клеток, проходящих затем последовательные стадии дифференцировки с
персистирующим, репликативно неактивным вирусом.
После инфицирования ВПЧ в клетках эпидермиса нарушается нормальный процесс
дифференцировки, особенно это касается клеток шиповатого слоя, в котором
наблюдается клональная экспансия инфицированных ВПЧ клеток базального слоя,
прошедших только первичную стадию дифференцировки. Эта клональная экспансия
связана с их трансформацией и последующей иммортализацией. Трансформация и
иммортализация клеток эпидермиса контролируется генами ВПЧ, кодирующими ранние
(early) белки Е6 и Е7. При этом наблюдается деформация внутренних слоев
эпидермиса и утолщение кожи, а клетки шиповатого слоя при переходе в зернистый
оказываются наиболее активными в синтезе ДНК. Эта фаза жизненного цикла ПВИ
включает второй этап репликативной дессиминации вируса внутри эпидермиса, в
результате чего значительно поражается зернистый слой эпидермиса, при
отсутствии экспрессии поздних (late) генов L1 и L2. Последняя, как показано,
наступает на конечной стадии дифференцировки в ороговевающем слое, где и
наблюдается активная сборка зрелых вирусных частиц, их выделение из клетки и
почкование прямо на поверхности кожи. Именно эти участки кожи инфекционно
опасны в отношении контактного заражения.
Иммунный ответ хозяина играет важную роль в предотвращении клинической
манифестации ВПЧ-инфекции. ВПЧ вызывает как гуморальный, так и клеточный типы
иммунного ответа. Клеточный иммунитет, особенно Т-клеточная иммунная система,
играет основную роль как в персистенции очагов ПВИ, так и в их спонтанном
регрессе, который имеет место в 90% случаев и может наступить через 6–8
месяцев после начала заболевания.
Роль иммунных нарушений в патогенезе ВПЧ-инфекции подтверждается данными о
более высокой частоте ВПЧ-ассоциированных заболеваний у реципиентов
трансплантата внутренних органов [12] и ВИЧ-инфицированных [20], обнаружении
нарушения Т-клеточного иммунитета у больных с генитальными бородавками,
снижении количества клеток Лангерганса в очагах цервикальной
интраэпителиальной неоплазии, а также большим количеством CD4+ и
CD8+ Т-лимфоцитов в инфильтрате регрессирующих генитальных
бородавок [21], предотвращении ВПЧ-инфицирования экспериментальных животных и
развития у них опухолевого процесса после иммунизации неструктурными белками
ВПЧ (Е6 и Е7) [14].
Важная роль клеточного звена иммунитета в патогенезе ВПЧ-инфекции также
подтверждается данными о полной ремиссии ВПЧ-ассоциированных заболеваний после
специфической стимуляции Т-клеточного иммунного ответа на гиперэкспрессию
онкобелков Е6 и Е7 (гиперэкспрессия онкобелков Е6 и Е7 на клеточной
поверхности возникает при интеграции ВПЧ в геном клетки) [8, 19].
В этой связи важно отметить, что онкобелки Е6 и Е7 довольно иммуногенны,
хорошо распознаются Т-лимфоцитами и проявляют свой эффект через формирование
комплексов со специфическими белками — р53 и Rb, которые обычно выполняют в
клетке противоопухолевую функцию. У вирусов с высоким онкогенным потенциалом
комплексы Е6-р53 и Е7-Rb более стабильны, а инфицированные вирусом клетки
неотвратимо становятся раковыми.
Клинически выделяют 4 типа генитальных бородавок.
- Остроконечные кондиломы — наиболее частая разновидность
генитальных бородавок. Это мягкие папилломатозные фиброэпителиальные
разрастания, по внешнему виду напоминающие цветную капусту, часто с
мацерированной поверхностью, поражающие, как правило, слизистые оболочки
(головка полового члена, наружное отверстие уретры, внутренний листок
крайней плоти, малые половые губы, вход во влагалище, шейка матки, анус и
анальный канал), реже — ороговевший эпителий (пах, промежность, перианальная
область). На слизистых оболочках они более плоские. При гистологическом
исследовании роговой слой состоит из паракератотических клеток, зернистый
слой отсутствует. Эпидермис в состоянии акантоза и резко выраженного
папилломатоза с утолщением и удлинением ветвящихся эпителиальных выростов;
характерна вакуолизация верхних слоев эпидермиса. Дерма резко отечная,
сосуды ее расширены; отмечаются очаговые воспалительные инфильтраты. В ряде
случаев остроконечные кондиломы могут трансформироваться в гигантскую
кондилому Бушке–Левенштейна.
- Кератотические бородавки — папулы, имеющие роговой вид и часто
напоминающие цветную капусту или себорейный кератоз, обычно располагающиеся
на коже ствола полового члена, мошонки, половых губ, паховых складок.
- Папулезные бородавки — куполообразные папулы диаметром от 1 до
4 мм с гладкой поверхностью (менее роговой, чем кератотические), имеющие
цвет сырого мяса и располагающиеся на коже, покрытой полностью ороговевшим
эпителием.
- Плоские бородавки — пятнистые элементы или слегка приподнятые
папулы, обычно невидимые невооруженным глазом, располагающиеся на фоне
частично или полностью ороговевшего эпителия.
Без лечения генитальные бородавки могут спонтанно инволюцировать (в 90%
случаев), длительно персистировать или увеличиваться в размере и количестве,
трансформируясь в рак (10%). Рак in situ без лечения переходит в инвазивный
рак в 36% случаях за 3,8–5,7 года [18]. С меньшей частотой спонтанной
инволюции подвергаются более длительно существующие очаги поражений.
Отсутствие спонтанной инволюции генитальных бородавок также может быть связано
с повторным инфицированием новыми типами ВПЧ. Реинфекция же одним и тем же
типом ВПЧ встречается не часто, возможно благодаря приобретенному иммунитету.
Прогноз генитальных бородавок зависит от типа обусловливающих их ВПЧ,
сопутствующих заболеваний (включая ИППП). Если ВПЧ 16 обычно приводит к
развитию плоскоклеточного рака, то ВПЧ 18 — к развитию аденокарценомы шейки
матки — формы рака с очень плохим прогнозом. Плохим прогностическим фактором
является и молодой возраст пациентки [10].
Для выявления ВПЧ-инфекции чаще всего применяются молекулярно-генетические
методы: неамплификационные (дот-блот, саузерн-блот гибридизация, гибридизация
in situ на фильтре и ткани) и амплификационные (ПЦР и HC-анализ (Hybrid
Capture)). При сравнении эффективности методов цервикальной цитологии и ПЦР в
обнаружении ВПЧ-инфекции установлено, что ПЦР-метод является более
чувствительным, чем цитологический.
В то же время ценность ВПЧ-типирования в клинической практике все еще не
совсем ясна. Во всяком случае, положительные результаты не являются
определяющими в предсказании исхода этой инфекции. Это связано как с
возможностью технических ошибок при выявлении ВПЧ высокого риска, так и с
необходимостью тщательного наблюдения за лицами с обнаруженными у них ВПЧ
среднего и высокого риска, поскольку клинические и гистологические признаки
ВПЧ-инфекции развиваются через 1–8 месяцев после первоначальной экспозиции
вируса и даже нелеченные элементы могут регрессировать спонтанно, длительно
существовать как доброкачественные или прогрессировать в предраковые поражения
и рак.
Для использования в скрининге и мониторинге терапии тестирования на ДНК ВПЧ
и для уверенности в надежности результатов используемый тест должен отвечать
ряду требований. Это выявление широкого спектра генотипов ВПЧ высокого
онкогенного риска (не менее 10 высокораспространенных) и невыявление
низкоонкогенных типов ВПЧ, снижающих специфичность исследования. Кроме того,
важной задачей ВПЧ-теста является возможность определения вирусной нагрузки.
При этом выявление вируса в количестве, не превышающем порогового, имеет малое
клиническое значение, так как говорит о высокой вероятности спонтанного
излечения. При этом как положительные должны учитываться только случаи
вирусной нагрузки, превышающей порог. В то же время при послеоперационном
мониторинге введение порога неоправданно, поскольку выявление вируса даже с
низкой нагрузкой может быть маркером рецидива [9].
Несмотря на то, что генитальные бородавки редко персистируют, а тем более
увеличиваются в размере и количестве и обычно регрессируют спонтанно,
выраженный онкогенный потенциал целого ряда типов ВПЧ, особенно в условиях
иммуносупрессии, ставит проблему лечения генитальных бородавок в разряд весьма
актуальных проблем современной медицины.
Исходя из биологических особенностей ПВИ, помимо удаления генитальных
бородавок большое внимание должно быть уделено лечению субклинической и
латентно протекающих ВПЧ-инфекций. Кроме того, решающее значение для
предотвращения рецидива и приостановления процесса канцерогенеза имеет
элиминация ВПЧ.
В настоящее время эффективность различных методов лечения генитальных
бородавок, даже с учетом проведения повторных курсов, составляет 60–80% [13].
Рецидивы в 25–50% случаев наступают в течение первых трех месяцев после
лечения и чаще всего обусловлены реактивацией вируса.
Поскольку в большинстве случаев больные с генитальными бородавками страдают
и другими ИППП, их половые партнеры должны быть также соответствующим образом
обследованы, в том числе на ВПЧ и ВИЧ-инфекции. Лечение генитальных бородавок,
как и других ИППП, следует проводить обоим половым партнерам, причем в период
его проведения им следует воздерживаться от половой жизни. После окончания
лечения необходима барьерная контрацепция в сроки до 6 месяцев.
При разработке стратегии лечения важно учитывать возраст больного,
локализацию, количество элементов, площадь очагов поражения, частоту
рецидивов, наличие сопутствующей соматической патологии (в том числе
урогенитальных инфекций), переносимость метода лечения, а также клинический
опыт врача.
Наиболее часто применяются следующие методы лечения остроконечных кондилом.
1. Физические методы:
- криодеструкция;
- электрокоагуляция;
- лазерная вапоризация.
2. Химическая цитодеструкция:
- подофиллотоксин;
- Подофиллин;
- трихлоруксусная кислота.
3. Антивирусная и иммуномодулирующая химиотерапия:
- Цидофовир;
- имиквимод;
- интерфероны (ИНФ) альфа-2 и гамма;
- блеомицин;
- фторурацил;
- ретиноиды.
4. Фотодинамическая терапия:
- с внутривенным применением фотосенсибилизатора;
- с местным применением фотосенсибилизатора.
В большинстве случаев бывает достаточно криодеструкции, электрокоагуляции,
лечения лучами лазера или фотодинамической терапии (ФДТ).
При распространенном, рецидивном процессе более эффективна комбинация
местного и общего лечения. При этом обычно вначале проводится деструктивное
лечение. Затем, в связи с тем, что латентная стадия жизненного цикла ВПЧ
протекает в клетках базального слоя эпидермиса и физическими методами очаг
поражения трудно удалить полностью (ДНК ВПЧ могут быть на расстоянии до 1 см
от видимых границ опухоли), сразу после регенерации эпидермиса, во избежание
рецидива, осуществляется противовирусная терапия препаратами ИНФ или кремом
имиквимод. В случае рецидива применяют антивирусные и иммунотропные препараты.
Все ИНФ эффективны в отношении ВПЧ. При остроконечных кондиломах их
применяют (инъекции внутрь очага или системно) в качестве терапии резерва,
особенно при отсутствии эффекта от общепринятой терапии. ИНФ — это цитокины
первой фазы иммунного ответа, обладающие антивирусными, антипролиферативными и
иммуностимулирующими свойствами благодаря способности усиливать
цитотоксическую активность Т-лимфоцитов и стимулировать их способность
уничтожать клетки с измененной антигенной структурой.
Как известно, большинство вирусов индуцирует синтез ИНФ (альфа и бета),
обладающих выраженной противовирусной и иммуномодулирующей активностью. В
клинической практике при лечении ВПЧ-ассоциированных заболеваний широко
используется ИНФ альфа-2.
Внутриочаговые инъекции под основание генитальных бородавок проводят
препаратами ИНФ альфа-2 в дозе 5 млн МЕ 3 раза в неделю в течение 3 недель.
ИФН применяют также с целью предварительной терапии крупных очагов поражения
для уменьшения их площади перед деструктивным методом, а также с целью
профилактики рецидивов [17].
Необходимо отметить техническую трудность проведения местного обкалывания
генитальных бородавок, выраженный гриппоподобный синдром при парентеральном
введении ИНФ, а также выраженную болезненность при проведении таких
манипуляций.
 Подобных
недостатков лишен препарат рекомбинантного ИНФ альфа-2 Виферон. В его состав
входят мембраностабилизирующие препараты — антиоксиданты — витамины Е и С в
терапевтически эффективных дозах. Это усиливает противовирусную и
иммуномодулирующую активность препарата в 10–14 раз по сравнению с препаратом
ИНФ альфа-2b Реафероном [2]. Применение его позволяет снизить суточную дозу
ИНФ при однократном введении и пролонгировать его действие. Лекарственная
форма препарата — ректальные суппозитории — также обеспечивает уменьшение
побочных реакций, характерных для парентерального введения препаратов ИНФ,
таких как повышение температуры, гриппоподобный синдром, и, кроме того,
придает препарату новые фармакокинетические свойства: при сравнении титров ИНФ
в сыворотке крови здоровых добровольцев при внутривенном, внутримышечном и
ректальном с антиоксидантами введении рекомбинантного ИНФ альфа-2b отмечено,
что при введении 1 млн МЕ ИНФ ректально титр ИНФ в сыворотке крови превышал
таковой при внутривенном или внутримышечном введении 2 млн МЕ ИНФ [4].
Существенно, что даже при длительном применении Виферона (в течение 2 лет) не
образуется антител, нейтрализующих антивирусную активность ИНФ альфа-2b [6].
Подобных
недостатков лишен препарат рекомбинантного ИНФ альфа-2 Виферон. В его состав
входят мембраностабилизирующие препараты — антиоксиданты — витамины Е и С в
терапевтически эффективных дозах. Это усиливает противовирусную и
иммуномодулирующую активность препарата в 10–14 раз по сравнению с препаратом
ИНФ альфа-2b Реафероном [2]. Применение его позволяет снизить суточную дозу
ИНФ при однократном введении и пролонгировать его действие. Лекарственная
форма препарата — ректальные суппозитории — также обеспечивает уменьшение
побочных реакций, характерных для парентерального введения препаратов ИНФ,
таких как повышение температуры, гриппоподобный синдром, и, кроме того,
придает препарату новые фармакокинетические свойства: при сравнении титров ИНФ
в сыворотке крови здоровых добровольцев при внутривенном, внутримышечном и
ректальном с антиоксидантами введении рекомбинантного ИНФ альфа-2b отмечено,
что при введении 1 млн МЕ ИНФ ректально титр ИНФ в сыворотке крови превышал
таковой при внутривенном или внутримышечном введении 2 млн МЕ ИНФ [4].
Существенно, что даже при длительном применении Виферона (в течение 2 лет) не
образуется антител, нейтрализующих антивирусную активность ИНФ альфа-2b [6].
При лечении эндоуретральных кондилом используют ежедневные инстилляции ИФН
альфа-2 в дозе 25 млн МЕ в течение 6 недель и с цитологическим контролем через
2 и 6 недель после окончания курса лечения, а затем — каждые 3 месяца в
течение года. Рецидив служит показанием к проведению повторного курса лечения
[17].
 По
нашему мнению, для лечения эндоуретральных кондилом наиболее оправдано
использование геля Виферон. Основной компонент препарата — человеческий
рекомбинантный ИНФ альфа-2 обладает выраженным противовирусным действием.
Природный антиоксидант — витамин Е и его синергисты — бензойная и лимонная
кислоты, метионин — способствуют стабилизации клеточных мембран, обладают
ранозаживляющим действием. Гелевая основа обеспечивает пролонгацию воздействия
препарата, а вспомогательные вещества — стабильность специфической активности
и надлежащую микробиологическую чистоту препарата.
По
нашему мнению, для лечения эндоуретральных кондилом наиболее оправдано
использование геля Виферон. Основной компонент препарата — человеческий
рекомбинантный ИНФ альфа-2 обладает выраженным противовирусным действием.
Природный антиоксидант — витамин Е и его синергисты — бензойная и лимонная
кислоты, метионин — способствуют стабилизации клеточных мембран, обладают
ранозаживляющим действием. Гелевая основа обеспечивает пролонгацию воздействия
препарата, а вспомогательные вещества — стабильность специфической активности
и надлежащую микробиологическую чистоту препарата.
Под нашим наблюдением находилось 18 пациентов (12 мужчин и 6 женщин) с
диагнозом «остроконечные кондиломы аногенитальной области». Возраст пациентов
варьировал от 19 до 38 лет и в среднем составлял 24,7 года. Для идентификации
типа ВПЧ в каждом случае проводилась ПЦР, необходимо отметить, что наиболее
часто выявлялись ВПЧ 6, 11, 31 и 33 типов, при этом в группе женщин из 6
пациенток у 5 был выявлен ВПЧ 6 типа. Все пациенты ранее неоднократно
проходили лечение по поводу остроконечных кондилом с применением различных
методов деструкции: электрокоагуляция, криодеструкция, лазерная вапоризация и
др. В среднем количество рецидивов составляло 2,8, при этом средний
межрецидивный период составлял 2,1 месяца и ни в одном случае его
продолжительность не превышала 4 месяцев.
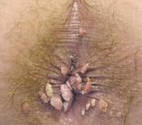
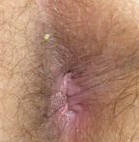
Всем пациентам проводился 14-дневный курс терапии ректальными
суппозиториями Виферон по 3 млн МЕ в сутки, местно применялся гель Виферон. На
15 день проводилась деструкция новообразований методом электрокоагуляции,
после чего рекомендовалось продолжить применение ректальных суппозиториев
Виферон по 1 млн МЕ в сутки в течение еще 15 дней. Ближайшие результаты
лечения в каждом случае были хорошими (рис. 1, 2). В период наблюдения в
течение не менее 8 месяцев рецидивов заболевания не было ни в одном случае.
Особо необходимо отметить хорошую переносимость применявшихся препаратов,
поскольку побочных эффектов или осложнений также не наблюдалось.
Полученные результаты позволяют рассматривать Виферон как эффективный
препарат для иммунотерапии ВПЧ-ассоциированных генитальных неоплазий и
рекомендовать его широкое внедрение в практику специалистов.
Литература
- Давыдов М., Демидов Л., Поляков В. Современное состояние и проблемы
онкологии // Врач. 2007. № 13. С. 3–7.
- Деленян Н. В., Ариненко Е. Н., Мешкова Е. Н. и др. Виферон. Руководство
для врачей / Под ред. В. В. Малиновской. М., 1997.
- Дмитриев Г. А., Биткина О. А. Папилломавирусная инфекция. М.:
Медицинская книга. 2006.
- Джуминго П. А. ИНФообразование и продукция специфических антител в
процессе комбинированной терапии реафероном и антиоксидантами у больных
простым рецидивирующим герпесом / Дисс… канд. мед. наук. М., 1990.
- Евстигнеева Н. П. Папилломавирусная инфекция урогенитального тракта
женщин: эпидемиология, факторы персистенции, оптимизация ранней диагностики
и профилактики онкогенеза / Автореф. дис..докт. мед. наук. М., 2007.
- Ершов Ф. И. Система ИНФа в норме и при патологии. М., Медицина, 1996.
- Киселев В. И. Вирусы папилломы человека в развитии рака шейки матки. М.:
Димитрейд График Групп, 2004.
- Киселев В. И., Киселев О. И. Вирусы папилломы человека в развитии рака
шейки матки. С.-Пб, М., 2003.
- Куевда Д. А. Современная концепция диагностики папилломавирусной
инфекции. Тез. докл. Межрегиональной научно-практической конференции «Дерматовенерология
в период реформирования здравоохранения и реализации национальных проектов».
Екатеринбург, 22–23 мая 2007. C. 112–113.
- Мазуренко Н. Н. Роль вирусов папилломы в канцерогенезе шейки матки //
Современная онкология. 2003. № 1. С. 7–10.
- Allen A. L., Siegfried E. C. What’s new in human papillomavirus
infection // Curr Opin Pediatr. 2000; 12: 365–369.
- Benton С., Shahidullah H., Hunter J. A. A. Human papillomavirus in the
immunosuppressed // Papillomavirus Rep. 1992. Vol. P. 23–26.
- Berman B., Ramires C. C. Anogenital warts / Treatment of Skin Disease /
Compehansive therapeutic strategies / Ed. M. G. Lebwohl et al. 2 nd ed.
2006. Mosbi. P. 47–49.
- Brandsma J. L. Animal models for HPV vaccine development //
Papillomavirus Rep. 1994. Vol. 5. P. 105–111.
- Greenfield I., Cutill S. Antivirals / Human papillomavirus. Clinical and
scientific advances / Ed. J. C. Sterling & S. K. Tyring-london: Arnold.
2001. P. 1120–1130.
- Kirnbauer R., Lenz P., Okun M. M. Human papilllomavirus In Dermatology /
Ed. J. L. Bolognia et al. Edinburg-Mosby. 2002. P. 1217–1234.
- Koutsky L. A., Kiviar N. B. Genital human papilomavirus. In: Sexual
Transmitted Diseases / Ed. K. K. Holmes et al. 3 rd ed. Mc. Growhill., New
York, 1999. P. 347–360.
- Munoz N. Human papillomavirus and cancer: the epidemiological evidence
// J. Clin. Virol. 2000. Vol. 19. P. 1–90.
- Munger K., Howley P. M. Human papillomavirus immortalization and
transformation functions // Virus Res. 2002. Vol. 89. P. 213.
- Palefski J. M. Anal sguamous cell intraepithelial lesions: relation to
HIV and human papillomavirus infection // J. Acquir. Immun. Defic. Syndr.
1999. Vol. 21 (Suppl.). Р. 42–48.
- Tagami H. Regression phenomenon of numerous Hat wars — An experiment on
the nature of tumor immunity in man // Int. J. Dermatol. 1983. Vol. 22. P.
570–571.
- Wiley D. J., Douglas J., Beutner K. et al. External gеnital warts:
diagnosis, treatment? And prevention // Clin. Inf. Dis. 2002. Vol. 35. P.
210–224.
- Zur Hauzen H. Papillomavirus infection- a major cause of human cancer //
Byochem. Biophys. Acta. 1996. Vol. 1288. F. 55–78.

