Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Этиологическая структура и антибиотикочувствительность
возбудителей острого необструктивного пиелонефрита у детей
М. И. Коган, доктор медицинских наук, профессор
Ю. Л. Набока, доктор медицинских наук, доцент
Л. И. Васильева, доктор медицинских наук, профессор
И. А. Гудима, кандидат медицинских наук
РостГМУ, Ростов-на-Дону
Инфекционно-воспалительные заболевания мочевой системы у детей,
в том числе и острый необструктивный пиелонефрит (ОНП), являются одной из
актуальных проблем детской урологии и нефрологии и характеризуются
этиологической мультифакторностью. Из микробных факторов наиболее полно изучены
бактериальные патогены с доминированием представителей семейства
Enterobacteriaceae. Этиологически причастными к формированию ОНП у детей могут
быть грампозитивная флора, неферментирующие грамотрицательные бактерии (Pseudomonas
sp.), а также другие бактериальные и вирусные патогены [1, 2, 3, 4, 5, 6].
Воспалительные заболевания органов мочевой системы, в том числе почек, могут
быть вызваны моно- и микст-инфекцией.
Лечение ОНП у детей в подавляющем большинстве случаев основано
на использовании антибактериальной терапии, которая нередко затруднена за счет
морфологических и функциональных особенностей почек и мочевыводящей системы,
способствующих селекции штаммов микроорганизмов, устойчивых к бактерицидному
действию гуморальных факторов защиты [4].
Целью данной работы явилось изучение антибиотикочувствительности
штаммов бактерий, этиологически причастных к формированию ОНП у детей, для
проведения адекватной антибиотикотерапии.
Материалы и методы
Были обследованы 60 детей с ОНП в возрасте от 6 месяцев до 12
лет. У 81,0% пациентов с ОНП развился на фоне инфекционных заболеваний
дыхательного и кишечного трактов. В 19,0% случаев заболевание возникло без
видимого разрешающего фактора. Для определения уровня бактериурии на
исследование забирали среднюю порцию утренней мочи. Исследуемый материал
доставляли в лабораторию в течение 1 часа. Количественный и качественный состав
микрофлоры мочи определяли на следующих питательных средах: Эндо, Сабуро,
желточно-солевой агар, 10% кровяной агар, приготовленный на основе агара
Мюллера–Хинтона с добавлением бараньих эритроцитов, среда КАБ, Блаурокка. Посевы
инкубировали в аэробных и анаэробных (10% CO2, 10% H2, 80% N2) условиях в
течение 2–4 суток. Идентификацию выделенных микроорганизмов осуществляли по
морфологическим, тинкториальным, культуральным и биохимическим признакам с
помощью Lachema тест-систем. Чувствительность выделенных микроорганизмов к 36
антибактериальным препаратам различных групп определяли диско-диффузионным
методом в аэробных и анаэробных условиях культивирования [8, 9]. Для определения
чувствительности анаэробных микроорганизмов постановку индивидуальных
антибиотикограмм проводили на среде первичного выделения (среда Мюллера–Хинтона
с добавлением бараньих эритроцитов).
Результаты и обсуждение
При бактериологическом исследовании мочи 60 больных с ОНП в 8,3%
случаев бактериальные патогены отсутствовали, в 91,7% — уропатогены выделяли как
в моноварианте (33,3%), так и в ассоциациях (58,4%). Степень бактериурии не
зависела от вида возбудителя и варьировала от 105 до 1010 КОЕ/мл.
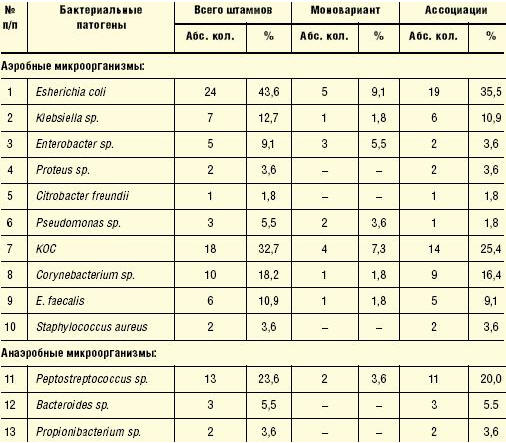
В этиологической структуре ОНП (табл. 1) доминировали
представители семейства Enterobacteriaceae (70,8%) с ведущей ролью эшерихий
(43,6%). Реже возбудителями ОНП были другие энтеробактерии: клебсиеллы (12,7%),
энтеробактеры (9,1%), протеи (3,6%), цитробактеры (1,8%). Удельный вес
представителей грамположительной микрофлоры (коагулазоотрицательные стафилококки
(КОС), коринеформные бактерии, энтерококки, золотистый стафилококк) составил
65,4% с преобладанием КОС (32,7%). Среди КОС доминировали Staphylococcus
haemolyticus (44,4%), S. epidermidis (33,3%). Реже из мочи выделяли S. warnerii
и S. hominis (по 11,1%). В таксономической структуре возбудителей ОП у детей
была выявлена значительная доля неклостридиальных анаэробов (НА) (32,7%) с
доминированием пептострептококков (23,6%). Пептострептококки в основном были
представлены видом Peptostreptococcus anaerobius (76,95), реже — P. productus
(23,1%). Значительно реже в моче регистрировали бактероиды (5,5%) и
пропионобактерии (3,6%).
Этиологическая структура ОНП бактериальной природы (n = 55)
В структуре бактериальных ассоциаций (рис.) доминировали
2-компонентные (51,4%) с основным ассоциантом Esherichia coli, реже выделяли
3-компонентные (37,1%), 4- и 5-компонентные (по 11,4%) ассоциации, с основным
ассоциантом пептострептококками.

Все выделенные из мочи штаммы проверяли на
антибиотикочувствительность к соответствующим препаратам. Данные по частоте
встречаемости чувствительных к антибиотикам возбудителей ОП у детей представлены
в табл.
2. Среди представителей семейства Enterobacteriaceae, выделенных из мочи,
резистентность эшерихий регистрировалась к 19 (52,8%) препаратам, энтеробактеров
— 24 (66,7%), клебсиелл — 25 (69,4%).
Из табл. 2 следует, что большинство штаммов энтеробактерий были
чувствительны к гентамицину, цефтазидиму. К антибиотикам пенициллинового ряда
был чувствителен лишь небольшой процент выделенных штаммов эшерихий: 16,7% к
ампициллину и 33,3% к азлоциллину. 100-процентную устойчивость представителей
семейства Епterobacteriaceae регистрировали к макролидам, карбенициллину,
оксациллину, доксициклину, цефиксиму, цефазолину, цефепиму, рифампицину,
фузидовой кислоте, нитроксолину.
Частота встречаемости (в %) чувствительных к антибиотикам
возбудителей ОНП у детей

Из цефалоспориновой группы антибиотиков более активными были
цефтриаксон в отношении E. coli (45,8%) и Enterobacter sp. (40,0%) и цефаклор —
для клебсиелл (28,6%) и энтеробактеров (20,0%).
По данным литературы [10, 11, 12], фторхинолоны являются одними
из лучших препаратов для лечения инфекций мочевыводящих путей (ИМВП), включая
ОНП, за счет высокой концентрации в ткани почек и моче, удобства применения,
активности в отношении большинства возбудителей ИМВП, бактерицидного эффекта и
относительно медленного развития резистентности. Однако в отношении последней
позиции эти же авторы указывают на то, что при осложненных ИМВП возможно быстрое
развитие резистентности к фторхинолонам, поэтому необходима постановка
индивидуальной антибиотикограммы [13].
К фторхинолонам (офлоксацин и норфлоксацин) были чувствительны
эшерихии (20,8 и 25,0–29,2% соответственно), энтеробактеры (60,0 и 40,0%),
клебсиеллы к норфлоксацину (42,8%).
Из антибиотиков других групп наибольшую активность проявлял
Тиенам: к эшерихиям — 41,7% и энтеробактерам — 40,0%. Энтеробактеры обладали
также чувствительностью к азтреонаму — 60,0% и меропенему — 40,0%.
Для КОС, выделенных из мочи детей с ОНП, прослеживалась
аналогичная тенденция множественной устойчивости к антибиотикам (19 (52,8%)
препаратов), как и для представителей семейства Enterobacteriaceae. Однако
наибольшей активностью обладали цефаперазон и ванкомицин (по 50,0%), цефотаксим,
цефазолин и Тиенам (по 44,4%), а также цефтриаксон, офлоксацин и меропенем (по
38,9%).
Выделенные из мочи штаммы коринебактерий (рис. 3) были устойчивы
к 24 (66,7%) препаратам. Наибольшая чувствительность регистрировалась к
цефтриаксону (60,0%), цефотаксиму (50,0%), ампициллину, цефоперазону,
цефокситину (по 40,0%).
Уропатогенные штаммы энтерококков обладали чувствительностью к
цефотаксиму, Тиенаму (по 66,7%) и цефтриаксону (50,0%). Псевдомонады были
чувствительны к Тиенаму (100,0%) и гентамицину (66,6%).
Из НА наибольший удельный вес в этиологии ОНП у детей имели
пептострептококки, которые также обладали множественной лекарственной
устойчивостью. Выраженной активностью по отношению к данным микроорганизмам
обладали Тиенам — 69,2%, цефотаксим — 61,5%, норфлоксацин и меропенем (по
53,8%). Все выделенные из мочи штаммы обладали 100% устойчивостью к 21 (58,3%)
из 36 антибактериальному препарату.
Таким образом, при первом эпизоде ОНП у детей большинство
выделенных из мочи уропатогенных бактерий обладают множественной лекарственной
устойчивостью. Для представителей семейства Enterobacteriaceae, вызывающих ОНП в
большинстве случаев, наиболее эффективными антибиотиками в рамках эмпирической
терапии являются гентамицин, цефтазидим и азтреонам, для КОС, энтерококков и
пептострептококков — Тиенам и цефотаксим. Обращает внимание, в целом, отсутствие
в ряду антибиотиков тех препаратов, которые бы оказывались эффективными в
большинстве клинических ситуаций ОНП. Фактически, в современных условиях
эмпирическая терапия способна элиминировать бактерии примерно в половине случаев
ОНП. Поэтому основное значение в излечении детей с ОНП должно принадлежать
этиотропной терапии. Вследствие этого, вырастает роль микробиологических методик
«быстродействия», то есть экспресс-диагностики. Мы полагаем, что современная
микробиология способна сделать окончательное заключение по микробному спектру
мочи уже к концу 4 суток. Этот срок, во-первых, позволяет оценить эффективность
эмпирической терапии, а во-вторых, более широко обследовать пациента для
исключения факторов, спровоцировавших ОНП и поддерживающих его. Роль
бактериологического исследования мочи при ОНП в настоящее время является еще
более значимой, чем прежде.
Литература
-
1. Гриценко В. А., Ляшенко И. Э., Гордиенко А. М. Информативность маркеров
персистенции E. coli при бактериологической диагностике хронического
пиелонефрита у детей // Журн. микробиол. 1996. № 3. С. 80–83.
-
2. Кузнецова А. Ю., Герасимчук А. Ф., Середа Т. А. Структура возбудителей
инфекций мочевыводящих путей в МСЧ «Северсталь» в 2003–2004 гг. // Мат.
научн. конф. «Узловые вопросы борьбы с инфекцией». СПб, 2004.С. 139–140.
-
3. Чернощекова К. А., Лепехина А. В., Чернощеков М. А. Происхождение
энтерококков // Мат. научн.-практ. конф. «Узловые вопросы борьбы с
инфекцией. СПб, 2004. С. 274.
-
4. Юшко Е. И. Инфекция мочевыводящих путей у детей: эпидемиология,
этиопатогенез, клиника, исходы и профилактика // Журн. урология. 2008. № 2.
С. 57–64.
-
5. Purcell K., Fergie J. Concurrent serious bacterial infections in 2396
infants and children hospitalized with respiratory syncytial virus lower
respiratory tract infections // Arch. Pediatr. Adolesc. Med. 2002. № 156
(4).
Р. 322–324.
-
6. Игнатова М. С. Новости педиатрической нефрологии с международного
конгресса нефрологов // Рос. вестн. перинатологии и педиатрии. 2004. № 1. С.
47–50.
-
7. Неймарк Б. А., Ефремов А. В., Исаенко В. А. Изменение свойств микрофлоры
мочи у больных с хроническим пиелонефритом разного возраста под влиянием
лазерного воздействия // Журн. «Эфферентная терапия». 2004. Т. 10. № 2. С.
32–36.
-
8. Меньшиков В. В. Справочник. Лабораторные методы исследования в клинике.
М., 1985.
-
9. Лабинская А. С., Волина Е. Г. Руководство по медицинской микробиологии.
М: БИНОМ. 2008. С. 280.
-
10. Яковлев С. В. Цефепим — цефалоспориновый антибиотик IV поколения //
Антибиотики и химиотерапия. 1999. № 7. С. 32–37.
-
11. Деревянко И. И. Применение цефепима (макситим) при лечении тяжелых
инфекций мочевыводящих путей // Антибиотики и химиотерапия. 2003. Т. 48. №
7. С. 24–28.
-
12. Рафальский В. В., Ходневич Н. В. Влияние резистентности возбудителей
инфекций мочевыводящих путей на исходы антибактериальной терапии // Журн.
урология. 2008.. № 4.С. 3–9.
-
13. Падейская Е. Н. Левофлоксацин в терапии урогенитальной инфекции //
Антибиотики и химиотерапия. 2004. Т. 49. № 6. С. 35–39.
Статья опубликована в журнале
Лечащий Врач

