Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Эффективность энтеросорбции в коррекции синдрома
эндотоксинемии при атопическом дерматите у детей
Б. А. Шамов, доктор медицинских наук, профессор
Т. Г. Маланичева, доктор медицинских наук, профессор
Казанский ГМУ, Казань
Непрерывный рост частоты атопического дерматита у детей,
нарастание тяжелых форм, приводящих к инвалидизации, резистентность к терапии
требуют поиска новых патогенетических механизмов в формировании данной
патологии. В качестве важного фактора, индуцирующего развитие различных
патогенетических процессов, в том числе и неинфекционных, является эндотоксин
грамотрицательных бактерий [1, 2].
В условиях патологической эндотоксинемии развивается клеточная
гипоксия, нарушаются метаболические процессы, активизируется симпатическая
нервная деятельность, система комплемента, приводящая к лизису лейкоцитов и
агрегации тромбоцитов с выходом биологически активных веществ (кинины, гистамин,
серотонин), что вызывает «медиаторный хаос» [3, 4]. Эндотоксиновая агрессия
квалифицируется как универсальный механизм, участвующий в патогенезе большинства
заболеваний инфекционного и неинфекционного генеза. Роль эндотоксиновой агрессии
в развитии различной патологии зависит от предрасположенности к заболеванию и
индивидуальных свойств инфекционного агента [5]. Все вышеизложенное позволило
нам предположить возможное наличие системной эндотоксинемии при атопическом
дерматите у детей.
Цель исследования — определить показатели плазменного
эндотоксина у детей с атопическим дерматитом для оптимизации методов терапии с
использованием энтеросорбентов.
Под наблюдением находилось 30 детей с атопическим дерматитом в
возрасте от 10 до 17 лет, которые составили основную группу. Мальчики составили
43%, девочки — 57%, дети в возрасте от 10 до 12 лет — 50%, от 13 до 17 лет —
50%. Детей с эритематозно-сквамозной формой с лихенификацией было 40%, с
лихеноидной формой атопического дерматита — 60%. Активность кожного процесса II
степени была у 40%, активность III степени — у 60% детей. Среднетяжелое течение
заболевания отмечалось у 67%, тяжелое — у 33% больных. У 67% пациентов
отмечалось повышение общего IgE в сыворотке крови.
Контрольную группу составили 20 практически здоровых детей. Из
них мальчиков — 40%, девочек — 60%, детей в возрасте от 10 до 12 лет — 50%, от
13 до 17 лет — 50%.
Эндотоксин определялся по методу Levin J., Bang F. B. LAL-тестом
(Limulus Amebocyte Lysate). Результаты выражались в международных единицах (МЕ).
Выявлено, что у детей, обследованных в период обострения
атопического дерматита, концентрация плазменного эндотоксина составила 0,140 ±
0,071 МЕ, тогда как в контрольной группе его значения составили 0,0024 ± 0,001
МЕ (р < 0,001). В период ремиссии показатели плазменного эндотоксина уменьшились
до 0,0178 ± 0,0138 МЕ (р < 0,05), при этом уровень эндотоксина превышал данные в
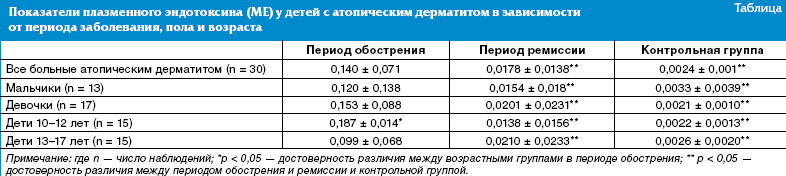
контрольной группе (р < 0,001). Уровень плазменного эндотоксина у детей с
атопическим дерматитом в зависимости от половой структуры и возраста представлен
в таблице.
При тяжелом течении атопического дерматита показатели
эндотоксина составили 0,168 ± 0,079 МЕ и значительно превышали показатели при
среднетяжелом течении — 0,076 ± 0,023 МЕ (р < 0,05). У детей с
эритематозно-сквамозной формой с лихенификацией и лихеноидной формой
атопического дерматита показатели эндотоксина почти не отличались и составили
0,123 ± 0,118 МЕ и 0,124 ± 0,077 МЕ соответственно. У детей со II степенью
активности кожного процесса концентрация эндотоксина была достоверно выше (0,143
± 0,092 МЕ), чем при III степени (0,112 ± 0,061 МЕ), р < 0,05.
Таким образом, при обострении атопического дерматита содержание
плазменного эндотоксина превышало контрольные показатели почти в 60 раз (р <
0,001), снизившись в 8 раз в период ремиссии (р < 0,05), однако его показатели
не достигли значений контрольной группы (р < 0,001). Определяемое содержание
эндотоксина у здоровых детей свидетельствует о наличии физиологической
эндотоксинемии.
Наличие системной эндотоксинемии является показанием для
проведения энтеросорбции [6] и включения в состав комплексной
противоаллергической терапии атопического дерматита препаратов, оказывающих
сорбционное, детоксикационное и цитопротекторное действие, а также благоприятно
влияющих на микрофлору кишечника. Таким лекарственным средством с комплексным
механизмом действия является препарат Энтеросгель. Энтеросгель является
селективным сорбентом нового поколения с высокой сорбционной способностью,
обладающим цитопротекторным действием на слизистую оболочку желудочно-кишечного
тракта, а также благоприятно влияющим на микрофлору толстого кишечника.
Для оценки эффективности энтеросорбции препаратом Энтеросгель
пациенты были разделены на две группы. В основную группу вошли 16 детей с
атопическим дерматитом, получающих в составе комплексной противоаллергической
терапии препарат Энтеросгель в течение 2 недель в возрастной дозировке: дети до
5 лет — по 1 чайной ложке 3 раза в день (15 г), от 5 до 14 лет — по 1 десертной
ложке 3 раза в день (30 г), старше 14 лет — по 1 столовой ложке 3 раза в день
(60 г). В группу сравнения вошли 14 детей, получавших традиционную
противоаллергическую терапию без препарата Энтеросгель. Традиционная терапия
между сравниваемыми группами не различалась и включала в себя гипоаллергенную
диету, антигистаминные препараты, наружную противовоспалительную терапию и
лечебно-косметический уход за кожей.
Выявлено, что в основной группе детей общий терапевтический
эффект составил 87,5%. Из них у 62,5% пациентов отмечалось клиническое
выздоровление. У 25% имело место значительное улучшение со стороны кожного
процесса. Это проявилось выраженной динамикой со стороны кожного процесса,
снижением индекса SCORAD более чем в 2,5 раза, а также снижением интенсивности
зуда, восстановлением ночного сна. Отсутствие эффекта отмечалось у 12,5%
больных. На фоне проводимой терапии отмечалось сокращение периода обострения, а
полное купирование морфологических элементов на коже и достижение клинической
ремиссии заболевания наблюдалось в среднем на 12 день от начала терапии. Индекс
SCORAD снизился в среднем по группе в 5 раз — с 50 до 10 баллов.
Среди пациентов группы сравнения общий терапевтический эффект
составил 64,3%. Из них у 42,9% пациентов отмечалось клиническое выздоровление. У
21,4% имело место значительное улучшение со стороны кожного процесса. Отсутствие
эффекта отмечалось у 35,7% больных. На фоне проводимой терапии индекс SCORAD
снизился в среднем в 3,3 раза — с 50 до 15 баллов. Достижение клинической
ремиссии заболевания наблюдалось на 20 день от начала терапии.
На фоне проводимой терапии отмечалось снижение уровня
плазменного эндотоксина в основной группе в 12 раз — с 0,142 ЕU до 0,012 ЕU,
тогда как в группе сравнения только в 6 раз — с 0,139 ЕU до 0,023 ЕU, р < 0,05.
Таким образом, у детей с атопическим дерматитом установлено
наличие системной эндотоксинемии. Причем содержание плазменного эндотоксина в
период обострения атопического дерматита превышает показатели в контрольной
группе, снижается в период ремиссии, но не достигает показателей физиологической
эндотоксинемии. Наличие синдрома системной эндотоксинемии является показанием
для проведения энтеросорбции. Назначение препарата комплексного действия
Энтеросгель в составе традиционной противоаллергической терапии приводит к
сокращению периода обострения в 1,7 раза (с 20 до 12 дней), снижению индекса
SCORAD в 5 раз на фоне снижения уровня плазменного эндотоксина.
Литература
-
Yakovlev M. Elements of Endotoxin Theory of Human Physiology and Pathology:
«Sistemic Endotoxinemia», «Endotoxin Agression» and «Endotoxin Insuficancy»
// J. of Endotoxin Research. 2000; 2: Р. 120.
-
Аниховская И. А., Опарина О. Н., Яковлева М. М. и др. Кишечный эндотоксин
как универсальный фактор адаптации и патогенеза общего адаптационного
синдрома // Физиология человека. 2006; 2: 87–91.
-
Вышегуров Я. Х, Аниховская И. А., Батманов Ю. Е. и др. Кишечный эндотоксин в
патогенезе воспалительной патологии глаза и антиэндотоксиновая составляющая
ее лечения // Патологическая физиология и экспериментальная терапия. 2007;
1: 12–14.
-
Таболин В. А., Лазарева С. И., Яковлев М. Ю. Антифосфолипидный синдром:
важная роль эндотоксиновой агрессии // Педиатрия. 2001; 5: 80–84.
-
Яковлев М. Ю. Элементы эндотоксиновой теории физиологии и патологии человека
// Физиология человека. 2003; 3: 154–164.
-
Чернихова Е. А., Аниховская И. А., Гатауллин Ю. К. и др. Энтеросорбция как
важное средство устранения хронической эндотоксиновой агрессии // Физиология
человека. 2007; 3: 135–136.
Статья опубликована в журнале
Лечащий Врач

