Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Математическое
моделирование моторно-эвакуаторных нарушений
желудочно-кишечного тракта у пациентов с язвенным
пилоро-дуоденальным стенозом
П.М. Косенко
1, С.А. Вавринчук 1, Л.К. КуликоВ
2, Е.С. Подвальный 3, А.В.
Плотников 4
ГБОУ ВПО «Дальневосточный государственный
медицинский университет», г. Хабаровск 1,
ГБОУ ДПО «Иркутская государственная медицинская
академия последипломного образования» 2,
ФГБОУ ВПО «Российская академия народного хозяйства и
государственной службы при Президенте Российской
Федерации» Воронежский филиал 3,
ФГБОУ ВПО «Воронежский государственный технический
университет», Российская Федерация 4
Цель. Улучшить диагностику язвенного
пилородуоденального стеноза путем создания
математической модели моторно-эвакуаторных нарушений
и автоматизированной компьютерной диагностической
системы.
Материал и методы. Обследовано 57
пациентов с язвенным пилородуоденальным стенозом,
разделенных по степени компенсации на 3 группы.
Контрольную группу составили 28 здоровых лиц. Оценка
моторики желудочно-кишечного тракта
выполнялась методом периферической
электрогастроэнтерографии. Математическое
моделирование моторно-эвакуаторных нарушений
выполнялось на основе дискриминантного анализа
показателей периферической электрогастроэнтерографии.
Результаты. Установлено, что группа
пациентов с субкомпенсированным пилородуоденальным
язвенным стенозом является неоднородной по характеру
нарушений моторики желудка с наличием переходных
типов от компенсации моторики (гипермоторный тип) к
декомпенсации (гипомоторный тип). На основе
дискриминантного анализа показателей периферической
электрогастроэнтерографии была создана
математическая модель моторно-эвакуаторных нарушений
желудочно-кишечного тракта у пациентов с язвенным
пилородуоденальным стенозом. Для улучшения
прогнозирования распределения пациентов в
соответствующие группы по степени тяжести стеноза
были использованы полученные нами ранее данные о
возрастных особенностях показателей периферической
электрогастроэнтерографии. В созданную
математическую модель вошло 23
электрофизиологических показателя, из которых
статистически значимыми для дифференциальной
диагностики оказались 17 показателей. Это обеспечило
высокую (96,2%) точность прогнозирования
распределения пациентов в соответствующие группы,
что позволило впервые создать компьютерную программу
диагностики и определения степени компенсации
пилородуоденального стеноза.
Заключение. На основе математической
модели прогнозирования моторно-эвакуаторных
нарушений у пациентов с язвенным пилородуоденальным
стенозом создана компьютерная система поддержки
принятия решения определения степени компенсации
пилородуоденального стеноза, позволяющая проводить
автоматизированный анализ данных периферической
электрогастроэнтерографии.
Ключевые слова: моторика
желудочно-кишечного тракта, язвенная болезнь,
дуоденальный стеноз, электрогастроэнтерография,
математическое моделирование, дискриминантный анализ
Введение
Пилородуоденальный стеноз (ПДС) является одним из
наиболее частых осложнений язвенной болезни
двенадцатиперстной кишки (ДПК), которое приводит к
нарушениям моторно-эвакуаторной функции (МЭФ)
желудка и ДПК у 10,0-56,3% пациентов с язвенной
болезнью (ЯБ) [1, 2].
Традиционно используемые рентгенологический и
эндоскопический методы диагностики
моторно-эвакуаторных нарушений желудочно-кишечного
тракта (ЖКТ) при язвенном ПДС имеют ряд существенных
недостатков (лучевая нагрузка, инвазивность,
косвенная оценка моторики, невозможность
использования в раннем послеоперационном периоде),
что не позволяет их использовать для своевременной
диагностики возникающих нарушений моторики
желудочно-кишечного тракта (ЖКТ) [1, 3, 4, 5, 6].
Наиболее информативным и доступным в клинической
практике современным методом изучения моторики ЖКТ,
отражающим непосредственную связь между изменениями
двигательной и электрической активности его отделов,
по всеобщему признанию, является периферическая
электрогастроэнтерография (ПЭГЭГ), которая не
инвазивна, не имеет противопоказаний и позволяет
получать информацию о состоянии всех отделов ЖКТ [1,
4, 5, 6, 7].
Имеются данные о применении ПЭГЭГ как при
хирургических заболеваниях, так и в терапевтической
гастроэнтерологии. При этом объектом интереса
исследователей являются не только отдельные
нозологии, но и функциональные нарушения, такие как
функциональная диспепсия, синдром раздраженного
кишечника и гастроэзофагеальный рефлюкс [1, 7, 8].
Однако, несмотря на все свои преимущества,
широкое внедрение ПЭГЭГ в клиническую практику
сдерживается сложностью оценки большого количества
взаимосвязанных электрофизиологических показателей и
отсутствием возможности их автоматизированного
анализа. Стандартная оценка показателей ПЭГЭГ с
визуальным описанием электрогастроэнтерограмм и
сравнением средних значений показателей ПЭГЭГ не
позволяет выявить многочисленные взаимозависимые
изменения моторики отделов ЖКТ, обусловленные
рефлекторным ответом на пищевую стимуляцию [1].
Одним из наиболее перспективных направлений
оптимизации анализа данных ПЭГЭГ является
моделирование систем и процессов путем создания
математических моделей (ММ) прогнозирования,
описывающих взаимосвязи между их ключевыми
показателями, в том числе и моторно-эвакуаторных
нарушений ЖКТ на основе статистических методов
прогнозирования [9, 10].
Однако, в настоящее время этот метод еще не
получил широкого распространения в клинических
исследованиях. В литературе отсутствуют сведения о
создании автоматизированных экспертных
диагностических систем по скринингу нарушений
моторики ЖКТ в автоматизированном режиме.
Цель. Улучшить диагностику язвенного ПДС
путем создания математической модели
моторно-эвакуаторных нарушений и автоматизированной
компьютерной диагностической системы.
Материал и методы
Обследовано 57 пациентов с язвенным ПДС. Мужчин
было 39 человек и женщин – 18. Средний возраст
пациентов составил 50,5±19,1 лет, средняя
продолжительность язвенного анамнеза 8,2±2,1 лет (M±σ).
Степень компенсации ПДС определяли по
классификации Ю.М. Панцырева и А.А Гринберга (1979)
[2]. Компенсированный ПДС был диагностирован нами у
25 (43,8%) пациентов, субкомпенсированный у 24
(42,1%) и декомпенсированный у 8 (14,1%)
обследованных. Контрольную группу составили 28
здоровых лиц.
Для электрофизиологической оценки состояния МЭФ
желудка и кишечника использовали ПЭГЭГ, которую
выполняли аппаратом "Гастроскан-ГЭМ" по стандартной
методике [1, 5].
При анализе ПЭГЭГ мы оценивали:
- суммарный уровень электрической активности (Ps)
органов ЖКТ;
- электрическую активность (ЭА) по отделам ЖКТ (Pi);
- процентный вклад каждого частотного спектра в
суммарный спектр (Pi/Ps) (%);
- коэффициент ритмичности (Критм), который
характеризует наличие и характер пропульсивных
сокращений гладкомышечных структур для каждого
отдела ЖКТ;
- коэффициент соотношения Pi/P(i+1) – отношение
ЭА вышележащего отдела к нижележащему.
Полученные нами результаты обследования пациентов
с субкомпенсированным ПДС отличались неоднородностью
изменений МЭФ желудка в этой группе пациентов, что,
по-нашему мнению, связано с наличием в этой наиболее
многочисленной группе пациентов переходных типов
нарушения моторики желудка от компенсации к ее
декомпенсации, которые не обнаруживаются стандартным
методом сравнения средних показателей ПЭГЭГ [1].
Для выявления переходных типов нарушений моторики
желудка у пациентов с субкомпенсированным ПДС, нами
был использован кластерный анализ, в который
включены 40 показателей ПЭГЭГ 24 пациентов с
субкомпенсированным ПДС. Мерой сходства между
объектами являлась метрика – евклидово расстояние
[11].
Для математического моделирования
моторно-эвакуаторных нарушений у пациентов с
язвенным ПДС на основе показателей ПЭГЭГ нами был
использован метод дискриминантного анализа (ДА),
который проводился путем пошагового включения
признаков в модель с итоговой оценкой вклада каждого
показателя в долю вероятности правильной
классификации [11].
Показателем информативности отобранных
дискриминантных переменных и полезности применения
дискриминантной функции для интерпретации
межгрупповых различий мы считали процент правильно
распознанных объектов с использованием вычисленных
дискриминантных функций.
Оценку вклада каждого показателя в дискриминацию
между группами проводили по показателю – частная
лямбда Уилкса. Чем меньше было значение частичной
лямбды Уилкса, тем большим был одиночный вклад
соответствующей переменной в степень дискриминации
[9, 10, 11].
Число правильно распознанных новых объектов, как
в целом, так и по отдельным группам,
свидетельствовало о соответствии дискриминантной
модели эмпирическим данным.
Математическое моделирование проводилось на
основе анализа 40 переменных (20 базальных и 20
стимулированных показателей ПЭГЭГ), полученных при
каждом исследовании.
ДА выполнялся методом пошагового исключения
показателей из модели по критериям Tolerance и
F-статистике (F для включения 1,6; F для исключения
1,5). Группирующим признаком являлась степень
компенсации ПДС.
Результаты
В результате кластеризации пациентов с
субкомпенсированным ПДС нами были выявлены 2 группы
(рис. 1). В первую группу вошли 10 (41,6%)
пациентов, которых мы соответственно выявленному
характеру изменений электрофизиологических
показателей обозначили как группу с гипомоторным
типом ПДС, и во вторую группу – 14 (58,3%)
пациентов, которых мы обозначили как группу с
гипермоторным типом ПДС.
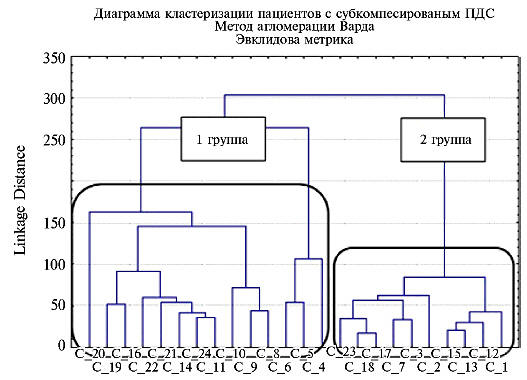
Рис. 1.
Дендрограмма объединения в кластеры пациентов с
субкомпенсированным ПДС
Анализ показателей ПЭГЭГ у пациентов с
гипермоторным типом субкомпенсированного ПДС показал
наличие у них крайней степени компенсации моторной
функции желудка, что проявлялось статистически не
значимым (p>0,05) повышением базальной электрической
активности (Pi, Pi/Ps) и перистальтической
активности (Kритм) желудка и кишечника со
значительным их возрастанием после пищевой
стимуляции (p<0,05).
Показатели ПЭГЭГ у пациентов с гипомоторным типом
субкомпенсированного ПДС отражали уже начальные
проявления декомпенсации моторики желудка, что
проявлялось повышением базального тонуса желудка и
его перистальтический активности (p<0,05) со
снижением этих показателей после пищевой стимуляции,
что по нашему мнению было обусловлено развитием
недостаточности нервно-мышечного аппарата желудка и
усугублением его двигательных расстройств.
На основе ДА нами была создана математическая
модель моторно-эвакуаторных нарушений у пациентов с
язвенным ПДС, включающая выявленные нами переходные
типы нарушения моторики желудка.
В результате анализа в созданную модель вошло 15
показателей ПЭГЭГ, из которых статистически
значимыми оказались 12 показателей (таблица 1).
Таблица 1.
Показатели ПЭГЭГ, дискриминирующие группы пациентов
с ПДС
|
|
Показатели
ПЭГЭГ |
Показатели
дискриминантного анализа |
|
Лямбда
Уилкса |
Частичная
Лямбда |
F статистика
(1,20) |
p |
Толерантность |
|
Ps (мВ)
|
Базал.
Стим.
Тощая кишка базал. |
0,048733
0,054987
0,042167 |
0,718624
0,636885
0,830517 |
4,796461
6,984231
2,499844 |
0,002
0,0001
0,054
|
0,042979
0,075177
0,139946 |
|
Pi (мВ) |
Тощая кишка стим.
Подвздошная кишка
стим. |
0,056474
0,044390 |
0,620117
0,788934 |
7,504323
3,277276 |
0,00008
0,01 |
0,019481
0,025521 |
|
Pi/Ps (%) |
Желудок стим. ДПК
стим. |
0,042522
0,046378 |
0,823582
0,755113 |
2,624053
3,972735 |
0,04
0,007 |
0,513080
0,191915 |
|
Pi/P (i+1) |
Желудок/ДПК базал.
ДПК/тощая кишка
стим.
Тощая/ Подвз.
базал.
|
0,046617
0,044581
0,041763
|
0,751242
0,785538
0,838557
|
4,056331
3,344399
2,358430
|
0,006
0,01
0,066
|
0,085807
0,298299
0,697858
|
|
Kритм |
Желудка базал.
ДПК базал.
ДПК стим.
Подвздошная кишка
стим.
Толстая кишка
базал. |
0,058469
0,046981
0,042050
0,044109
0,043269 |
0,598957
0,745420
0,832837
0,793961
0,809369 |
8,202235
4,183692
2,458762
3,178970
2,885240 |
0,00003
0,005
0,057
0,02
0,03 |
0,022811
0,050891
0,030605
0,026081
0,141796 |
Примечание: 25 Шагов, переменных в модели 15,
число групп – 5. Лямбда Уилкса: 0,03502 approx. F
(60,193)=4,3861; p< 0,0000.
Наибольший вклад в дискриминацию между
исследуемыми возрастными группами (по показателю
частичной лямбды Уилкса) внес базальный показатель
Критм желудка.
Использование полученных показателей для
прогнозирования моторно-эвакуаторных нарушений
показало достаточно высокую прогностическую
эффективность (85,2%) полученной модели (рис. 2).
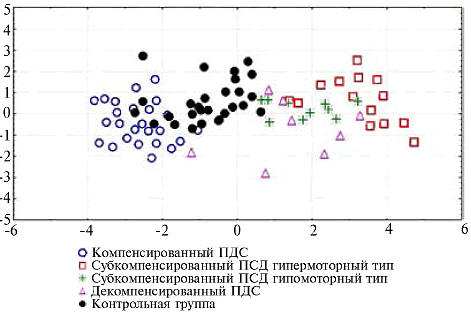
Рис. 2.
Распределение пациентов ЯБ, осложненной ПДС, и
контрольной группы на основании дискриминантного
анализа
Ранее нами уже были выявлены возрастные
особенности показателей ПЭГЭГ и показана
необходимость учета этих изменений [1]. В связи с
этим для улучшения результатов прогнозирования в
качестве контрольной группы была взята группа
здоровых людей, средний возраст которых составил
63±7,25 лет (M±σ). Контрольная группа (средний
возраст 63±7,25 лет) и группа сравнения (средний
возраст 57,5±13,7 лет) не имели статистически
значимых различий по возрасту.
В результате этого было отмечено изменение в
созданной математической модели. В нее вошло 23
показателя ПЭГЭГ, из которых статистически значимыми
для дифференциальной диагностики оказались 17
показателей (таблица 2).
Таблица 2.
Показатели ПЭГЭГ, дискриминирующие группы пациентов
с ПДС
|
|
Показатели
модели |
Показатели
дискриминантного анализа |
|
Лямбда
Уилкса |
Частичная
лямбда |
F статистика
(1,20) |
p |
Толерантность |
|
Ps (мВ) |
Базал.
Стим. |
0,009984
0,010782 |
0,562800
0,521127 |
5,049401
5,972963 |
0,003
0,001 |
0,00010
0,00748 |
| Pi (мВ)
|
Желудок базал.
Подвздошная кишка
базал.
Подвздошная кишка
стим.
Толстая кишка
базал. |
0,009187
0,011391
0,011234
0,010428 |
0,611597
0,493280
0,500158
0,538803 |
4,127920
6,677088
6,495900
5,563784 |
0,01
0,0007
0,0009
0,002 |
0,00063
0,00076
0,00555
0,00041 |
| Pi/Ps (%)
|
Желудок базал.
Желудок стим.
ДПК стим.
Тощая кишка стим.
Подвздошная кишка
базал.
Подвздошная кишка
стим.
Толстая кишка
базал. |
0,009611
0,007749
0,007852
0,007865
0,008328
0,008980
0,010377 |
0,584630
0,725072
0,715633
0,714439
0,674660
0,625714
0,541470 |
4,618146
2,464626
2,582869
2,598049
3,134483
3,888136
5,504353 |
0,005
0,07
0,06
0,051
0,03
0,01
0,002 |
0,02129
0,09847
0,04397
0,01820
0,08638
0,03464
0,01226 |
| Критм
|
Желудка базал.
Желудка стим.
ДПК базал.
Тощая кишка базал.
Подвздошная кишка
стим.
Толстая кишка
базал. |
0,007125
0,010436
0,010723
0,006926
0,010271
0,012999 |
0,788552
0,538402
0,523984
0,811287
0,547065
0,432267 |
1,742954
5,572756
5,904972
1,511960
5,381590
8,537013 |
0,1
0,002
0,001
0,2
0,002
0,0001 |
0,00652
0,00735
0,01628
0,00874
0,00619
0,00448 |
Примечание: 17 Шагов, переменных в модели 23,
число групп – 5. Лямбда Уилкса: 0,03502 approx. F
(60,193)=4,3861; p<0,0000
Использование в качестве группы сравнения нормы
для пожилых людей привело к значительному улучшению
прогностической эффективности созданной модели.
Общий процент правильной классификации наблюдений
в соответствующие группы составил 96,2% (рис. 3).
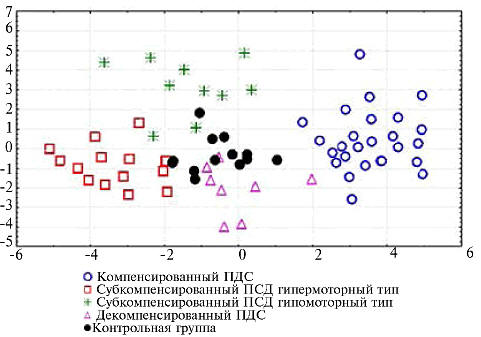
Рис. 3.
Распределение пациентов ЯБ, осложненной ПДС и
контрольной группы (пожилые лица) на основании
дискриминантного анализа
Значения чувствительности, специфичности и
точности ПЭГЭГ в диагностике ПДС на основе созданных
ММ составили 96,2%, 85,7% и 96,9% соответственно.
Обсуждение
Таким образом, в основе созданной ММ
моторно-эвакуаторных нарушений у пациентов с
язвенным ПДС на основе ДА показателей ПЭГЭГ, лежит
объективная связь моторики ЖКТ с нарушением пассажа
пищи, как основного ее стимулятора.
Включение в ММ электрофизиологических показателей
всех отделов ЖКТ позволяет учесть имеющиеся при этой
патологии закономерности изменения их моторики, а не
только изменение моторики желудка и ДПК.
Использование показателей «возрастной нормы»
позволяет улучшить прогностическую точность ММ. ММ
моторно-эвакуаторных нарушений у пациентов с ПДС
создает предпосылки к автоматизированному анализу
показателей ПЭГЭГ.
На основе полученных нами данных совместно с
сотрудниками кафедры автоматизированных и
вычислительных систем ФГБОУ ВПО «Воронежский
государственный технический университет» профессором
Е.С. Подвальным и аспирантом А.В. Плотниковым была
создана компьютерная программа «Система поддержки
принятия решения определения степени компенсации
пилоро-дуоденального стеноза» (свидетельство о
государственной регистрации программы для ЭВМ
№2013618128).
Сотрудники данной кафедры имеют приоритет в
создании компьютерных систем моделирования и
индивидуального прогнозирования состояний у
пациентов с различными заболеваниями.
Программа предназначена для работы в медицинских
учреждениях для установки диагноза ПДС и уточнения
степени его компенсации.
Программа имеет модульную структуру и включает
управляющий модуль, модули дис-криминантного
анализа, статистической обработки, установления
диагноза, визуализации, верификации модели и модуль
базы данных (БД) статистики.
Программа обеспечивает пользователю следующие
возможности:
- Установление диагноза ПДС и определение
степени его компенсации;
- Учет возрастных особенностей ПЭГЭГ –
дифференциация диагностики с учетом возраста
обследуемого;
- Возможность получать графики нелинейных
дискриминантных функций различных параметров в их
сочетании с отображением ин-дивидуальных
параметров пациента;
- Актуализация БД обучающей и контрольных
выборок для коррекции статистики.
Для установления диагноза программа использует
обучающую выборку, которая представлена в виде базы
данных и может быть дополнена новыми данными.
Увеличение обучающей выборки повышает точность
дис-криминантной модели и улучшает результаты
диагностики.
Заключение
Таким образом, полученные дискриминирующие
показатели ПЭГЭГ и созданная на их основе ММ
прогнозирования моторно-эвакуаторных нарушений у
пациентов с язвенным ПДС показали свою высокую
эффективность при скрининговой диагностике ПДС и
определении степени компенсации, что позволило
впервые осуществить автоматизированную компьютерную
скрининговую диагностику ПДС и определение степени
его компенсации.
ЛИТЕРАТУРА
- Вавринчук С. А. Системный анализ показателей
периферической электрогастроэнтерограффии у
больных с осложненной язвенной болезнью / С. А.
Вавринчук, П. М. Косенко. – Хабаровск : ИПКСЗ,
2012. – 189 с.
- Рухляда Н. В. Диагностика и лечение язвенной
болезни, осложннной стенозом / Н. В. Рухляда, В.
Е. Назаров, И. А. Ермолаев. – СПб. : ДЕАН, 2006. –
240 с.
- Yin J. Electrogastrography: methodology,
validation and applications / J. Yin, J. D. Chen
// J Neurogastro-enterol Motil. – 2013 Jan. – Vol.
19, N 1. – P. 5–17.
- Application of electrogastrography to public
health / Y. Matsuura [et al.] Nihon Eiseigaku
Zasshi. – 2011 Jan. – Vol. 66. N 1. – P. 54–63.
- Периферическая электрогастроэнтерография в
диагностике нарушений моторно-эвакуаторной функции
желудочно-кишечного тракта / В. А. Ступин [и др.]
// Лечащий врач. – 2005. – № 2. – С. 60–62.
- Теоретические предпосылки и экспериментальное
обоснование использования
электрогастроэнтерографии / Н. С. Тропская [и др.]
// Рос. журн. гастроэнтерологии, гепатологии,
колопроктологии. – 2005. – Т. 15, № 5. – C. 82–88.
- Периферическая электрогастроэнтерография в
диагностике ГЭРБ : пособие для врачей / О. Б.
Дронова [и др.]. – М. : ИД Медпрактика-М, 2011. –
32 с.
- Интестинальная двигательная активность у
пациентов с синдромом раздраженного кишечника / Е.
И. Ткаченко [и др.] // Гастроэнтерология С.-Петерб.
– 2008. – № 4. – С. 7–10.
- Семерякова Е. Г. Математические методы в
задачах медицинской диагностики / Е. Г. Семерякова,
О. Г. Берестнева, Л. С. Макарова // Соврем.
проблемы науки и образования. – 2012. – № 6. – С.
29.
- Вильдеман А. В. Многомерный метод
индивидуального прогнозирования индекса моторики /
А. В. Вильдеман, А. А. Ташкинов, В. А. Бронников
// Информац. технологии и вычисл. системы. – 2010.
– № 3. – С. 79–85.
- Реброва О. Ю. Статистический анализ
медицинских данных. Применение пакета прикладных
программ Statistica / О. Ю. Реброва. – М. :Медиасфера,
2002. – 312 с.
Статья опубликована на сайте
http://www.gastroscan.ru

