
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Изменения
миоэлектрической активности желудочно-кишечного
тракта у больных колоректальным раком, осложненным
перифокальным инфильтратом и абсцессом
Бабков О.В.1,
Рудаков Д.А.2, Луфт В.М.1,
Захаренко А.А.3, Безмозгин Б.Г.1,
Суров Д.А.2, Тен О.А., Лапицкий А.В.1
1 ГБУ «Санкт-Петербургский
научно-исследовательский институт скорой помощи
имени И.И. Джанелидзе», г. Санкт-Петербург, ул.
Будапештская дом 3; 8-911-281-31-97
2 Военно-медицинская Академия им. С.М.
Кирова, кафедра военно-морской и госпитальной
хирургии, г. Санкт-Петербург, ул. Ак. Лебедева, дом
6
3 Первый Санкт-Петербургский
государственный медицинский университет им. акад.
И.П. Павлова
Резюме: в статье рассмотрены вопросы
нутриционной поддержки больных колоректальным раком,
осложненным перифокальным инфильтратом и абсцессом,
а также описаны изменения миоэлектрической
активности желудочно-кишечного тракта у больных
данной категории на фоне применения нутриционной
поддержки и без нее.
Установлено, что применение описанного протокола
нутриционной поддержки позволяет нормализовать
миоэлектрическую активность кишечника, которая
является отражением его моторно-эвакуаторной
функции.
Ключевые слова: колоректальный рак,
перифокальный инфильтрат, абсцесс, нутриционная
поддержка, миоэлектрическая активность.
Введение
Колоректальный рак (КРР) объединяет различные по
форме, локализации и гистологической структуре
злокачественные эпителиальные опухоли ободочной и
прямой кишок. В мире регистрируется более 600 тысяч
случаев КРР ежегодно, в России более 50 тысяч
случаев впервые выявленного КРР и более 35 тысячи
смертей от него. В структуре заболеваемости
злокачественными новообразованиями населения России
колоректальный рак занимает второе место у мужчин
(10,9%) и третье место у женщин (11,9%) [9].
Прогрессирование заболевания приводит к снижению
иммунореактивности больных, развитию различных, в
том числе гнойно-воспалительных осложнений, которые
являются конкурирующими с опухолевым процессом
факторами, в ряде случаев, оказывающими более
негативное влияние на прогноз, чем прогрессирование
основного заболевания [5].
Около 89,0% больных КРР поступает в хирургические
стационары с различными осложнениями [6], к которым
относят обтурационную непроходимость (до 85,0% всех
осложнений), перфорацию опухоли с развитием
перитонита (2,1–27,0%), перифокальный воспалительный
инфильтрат и абсцесс (12,0–35,0%), а также кишечное
кровотечение (4,0–15,3%) [1,2].
По данным различных авторов у больных с осложненным
КРР наблюдается трофическая недостаточность
различной степени выраженности, которая усугубляется
в послеоперационном периоде, ухудшая
непосредственные результаты хирургического лечения
[4,10]. Это обусловливает необходимость проведения
нутриционной поддержки (НП) больных КРР, осложненным
перифокальным инфильтратом и абсцессом.
В тоже время в литературе достаточно скудно освещен
вопрос оценки эффективности влияния НП на
моторно-эвакуаторную функцию желудочно-кишечного
тракта (ЖКТ) у больных осложненным КРР в
послеоперационном периоде. В настоящий момент
электрогастроэнтерография (ЭГЭГ) привлекает внимание
специалистов, как метод неинвазивного исследования
функционального состояния ЖКТ, отражающий его
функциональные изменения и позволяющий осуществлять
длительные многократные исследования [7].
Материалы и методы
Исследование выполнено на основе анализа лечения 232
больных оперированных по поводу КРР, осложненного
перифокальным инфильтратом или абсцессом,
проходивших лечение в ГБУ НИИ скорой помощи им. И.И.
Джанелидзе в 2004-2013 годах. Контрольную группу
составляли 124 больных, проходивших лечение
2004-2008 годах. У 81 больного (65,3%) из этой
группы был выявлен перифокальный инфильтрат, а у 43
больных (34,7%) – перифокальный абсцесс. В
контрольной группе лечение проводилось традиционным
способом, без использования нутриционной поддержки.
Основную группу составили 108 больных, проходивших
лечения в 2009-2013 годах. Из них у 67 больных
(62,0%) был выявлен перифокальный инфильтрат, а у 41
больного (38,0%) – перифокальный абсцесс. Данным
больным помимо стандартной терапии проводились
мероприятия НП.
Контрольная и основная группы больных были идентичны
по полу, возрасту, длительности заболевания,
распространенности онкологического процесса,
характеру выполненных операции. Методика проведения
НП учитывала особенности данной категории больных,
наличие у них исходной кишечной недостаточности,
иммуносупрессии и заключалась в последовательной
смене различных питательных смесей: мономерная смесь
– полимерная изокалорическая изонитрогенная смесь –
гиперкалорическая иммунная смесь.
Нутриционная поддержка больных КРР, осложненным
перифокальным воспалительным инфильтратом и
абсцессом, включала в себя применение смесей для
энтерального питания методом сипинга в
периоперационном (пред- и послеоперационном)
периоде, использование антигипоксантов, специальной
иммунной смеси.
Искусственное лечебное питание у больных с
перифокальным инфильтратом начиналось в
предоперационном периоде и включало применение
больным перорально 12,0% раствора глюкозы в объеме
400,0 мл за 2 часа до операции, что позволяло
уменьшить предоперационную жажду, голод и
послеоперационную резистентность к инсулину, а также
снизить потери азота и белка [8].
При благоприятном течении послеоперационного
периода, в случае отсутствия явлений гастростаза, в
1 сутки послеоперационного периода НП включала в
себя пероральное применение больным 400,0 мл
глюкозо-электролитной смеси (ГЭС) следующего
состава: 1,0 л дистиллированной воды, 1 пакет (18,9
г) препарата «регидрон», 1,0 г аскорбиновой кислоты,
10,0 мл препарата «цитофлавин». Для обеспечения
внутрипросветной регенеративной трофики кишки и
сохранения кишечного барьера применялось минимальное
количество (200,0 мл) изокалорической изонитрогенной
смеси «нутризон-стандарт». В качестве энтеросорбента
использовали препарат «энтеросгель» двукратно по
30,0 г (как препарат, обладающий адсорбирующим и
дезинтоксикационным действием).
На вторые сутки послеоперационного периода
переходили на использование специальной
гиперкалорической иммунной смеси «нутриэн-иммун» в
объеме 600,0 мл.
Количество применяемой ГЭС и энтеросорбента при этом
оставалось прежним.
При хорошей переносимости больным питательной смеси
на третьи сутки количество используемой смеси «нутриэн-иммун»
увеличивали до объема 1000,0 мл.
Количество применяемой ГЭС и энтеросорбента
оставалось прежним. На четвертые сутки
послеоперационного периода назначался лечебный
рацион (диета № 1 по Певзнеру) с дополнительным
пероральным приемом смеси «нутриэн-иммун» по 200,0
мл 3 раза в день.
Таблица 1. Схема нутриционной
поддержки больных колоректальным раком, осложненным
перифокальным инфильтратом и абсцессом
Сутки
|
Мероприятия
нутриционной поддержки*
|
Продолжительность
|
2 часа
до операции
|
Раствор глюкозы 12% - 400 мл**
|
15 минут
|
1 сутки
200,0 ккал
|
ГЭС***– 200,0 мл + Нутризон-Стандарт –
100,0 мл
|
5 часов
|
8 г белка
|
Энтеросгель – 30 г
|
После НП
|
ГЭС – 200,0 мл + Нутризон-Стандарт – 100,0
мл
|
5 часов
|
Энтеросгель – 30 г
|
После НП
|
2 сутки
750,0 ккал
42 г белка
|
ГЭС – 200,0 мл + Нутриэн-Иммун
– 300,0 мл
|
5 часов
|
Энтеросгель – 30 г
|
После НП
|
| ГЭС – 200,0 мл + Нутриэн-Иммун
– 300,0 мл |
5 часов
|
Энтеросгель – 30 г
|
После НП
|
3 сутки
Нутриэн-Иммун
1250,0 ккал
70 г белка
|
ГЭС – 200,0 мл + Нутриэн-Иммун – 500,0 мл
|
5 часов
|
Энтеросгель – 30 г
|
После НП
|
ГЭС – 200,0 мл + Нутриэн-Иммун – 500,0 мл
|
5 часов
|
Энтеросгель – 30 г
|
После НП
|
4 сутки
Стол № 1
Нутриэн-Иммун
2000 ккал
|
Стол № 1 с дополнительным приемом
Нутриэн-Иммун
по 200,0 мл 3 раза в сутки методом сипинга
|
|
* - прием всех препаратов осуществляется
перорально
**- при перифокальном инфильтрате
*** ГЭС – 1,0 л дистиллированной воды, 1 пакет
регидрона, 1,0 г аскорбиновой кислоты, 10,0 мл «цитофлавин».
С целью сравнительной оценки влияния нутриционной
поддержки на моторно-эвакуаторную функцию ЖКТ нами
было произведено исследование миоэлектрической
активности различных отделов ЖКТ. Исследования
проводили у 24 больных основной и у 28 больных
контрольной групп на 1, 3 и 5 сутки
послеоперационного периода.
Регистрацию миоэлектрической активности проводили с
помощью гастроэнтеромонитора ГЭМ 01 "Гастроскан-ГЭМ".
В результате спектрального анализа полученных данных
рассчитывалась мощность электрического сигнала по
каждому частотному отделу Pi (т.е. по частотам,
характерным для желудка, двенадцатиперстной, тощей,
подвздошной и толстой кишки) и суммарная мощность Ps.
Суммарная мощность электрического сигнала (суммарная
электрическая активность) позволяла оценить уровень
базальной электрической активности. Отношение
абсолютных значений электрической активности в
каждом отделе ЖКТ к суммарной активности
представляет, достоверно стабильные относительные
показатели электрической активности. Оценка
указанных показателей позволяет в достаточной мере
достоверно судить о тонической и перистальтической
составляющих моторной функции желудочно-кишечного
тракта.
Для отработки исходно нормативных параметров
миоэлектрической активности различных отделов ЖКТ
была отобрана группа добровольцев в количестве 30
здоровых людей, возраст которых составлял от 57 до
74 лет (средний возраст - 72,1±4,3 лет).
Исследование проводилось в утренние часы, натощак,
на период исследования исключалось курение. Средние
показатели миоэлектрической активности различных
отделов ЖКТ в группе добровольцев приведены в табл.
2.
Таблица 2. Средние показатели
миоэлектрической активности ЖКТ
Отдел
|
Полученная
норма
|
Желудок
|
9,8±1,7 мВт |
Двенадцатиперстная кишка
|
0,8±0,2 мВт
|
Тощая кишка
|
2,6±0,7 мВт |
Подвздошная кишка
|
8,6±0,9 мВт |
Толстая кишка
|
16,1±1,7 мВт
|
Математическая обработка фактического материала
выполнялась с помощью программы IBM SPSS Statistics.
Критический уровень статистической значимости при
проверке нулевой гипотезы принимался равным 0,05.
Результаты
На 1 сутки отмечалось равномерное снижение
миоэлектрической активности ЖКТ у больных основной и
контрольной групп (желудок 4,7±1,2 мВт и 4,9±1,4
мВт; двенадцатиперстная кишка 0,3±0,11 мВт и 0,3±0,9
мВт; тощая кишка 0,5±0,2 мВт и 0,4±0,15 мВт;
подвздошная кишка 1,2±0,3 мВт и 1,1±0,45 мВт;
толстая кишка 2,9±0,55 мВт и 3,2±0,7 мВт,
контрольная и основная группы соответственно).
Различий между группами сравнений не было (р>0,05).
Данные представлены на рисунке №1.
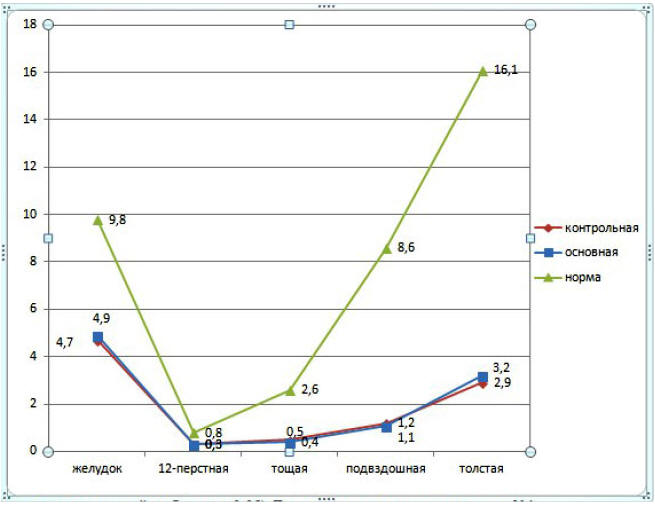
Рис. 1. Динамика изменений миоэлектрической
активности ЖКТ на первые сутки послеоперационного
периода
Однако уже к 3 суткам послеоперационного периода
показатели МЭА различных отделов ЖКТ у больных
основной группы сравнивались с нормальными
значениями, в то время как МЭА у больных контрольной
группы оставалась достоверно ниже (желудок 6,2±1,5
мВт и 9,1±1,1 мВт; двенадцатиперстная кишка 0,5±0,13
мВт и 0,9±0,2 мВт; тощая кишка 1,4±0,4 мВт и 2,9±0,6
мВт; подвздошная кишка 3,2±0,75 мВт и 7,6±1,5 мВт;
толстая кишка 7,7±1,2 мВт и 14±2,1 мВт, р<0,05).
Данные представлены на рисунке №2. На 5 сутки
послеоперационного периода исследуемый показатель в
группах сравнения соответствовал нормальным
значениям и достоверно друг от друга не отличался
(желудок 8,4±1,9 мВт и 11,1±2,1 мВт;
двенадцатиперстная кишка 0,9±0,3 мВт и 1,2±0,25 мВт;
тощая кишка 3,1±0,7 мВт и 3,2±0,8 мВт; подвздошная
кишка 7,3±1,1 мВт и 8,9±1,4 мВт; толстая кишка
16,3±2,2 мВт и 17,8±3,1 мВт; р>0,05). Данные
представлены на рисунке №3.

Рис. 2. Динамика изменений миоэлектрической
активности ЖКТ на третьи сутки послеоперационного
периода
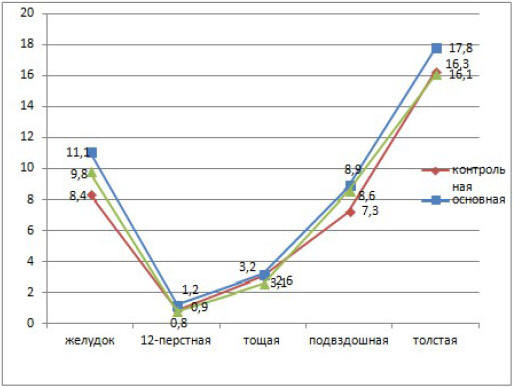
Рис. 3. Динамика изменений миоэлектрической
активности ЖКТ на пятые сутки послеоперационного
периода
Выводы
- У больных КРР, осложненным перифокальным
инфильтратом и абсцессом, в раннем
послеоперационном периоде имеет место значительное
снижение МЭА органов ЖКТ.
- Применение разработанной программы НП
позволяет уже к 3 суткам послеоперационного
периода нормализовать МЭА ЖКТ и, как следствие,
восстановить его моторно-эвакуаторную функцию.
Литература
- Антипова С.В., Калинин Е.В., Шляхтин В.В.
Алгоритм и методы хирургического лечения
осложненных форм колоректального рака //
Онкология. - 2009. - Т. 11, N 4. - С. 293-297.
- Безмозгин Б.Г. Динамика уровня эндогенной
интоксикации у больных колоректальным раком,
осложненным перитонитом / Б.Г. Безмозгин, О.В.
Бабков, Д.А. Суров, А.А. Захаренко, С.А.
Шляпников, В.Е. Савелло, О.А. Тен, А.А. Трушин,
И.М. Батыршин // Medline.ru. – 2013. – Т. 14.
Онкология. – С. 1100–1108.
- Луфт В.М. Нутриционная поддержка больных
колоректальным раком, осложненным перифокальным
воспалением и абсцедированием / В.М. Луфт, А.А.
Захаренко, Д.А. Суров, О.В. Бабков, А.В. Лапицкий,
Д.А. Рудаков, Б.Г. Безмозгин, О.А. Тен, Д.В.
Кодолов // Пособие для врачей. – СПб., 2013. – 14
с.
- Митрохин С.Д., Миронов А.Ю., Киямов А.Р.
Профилактика инфекций области хирургического
вмешательства у онкологических больных // Человек
и его здоровье. – 2012. - №2. - С. – 127-132.
- Обухова О.А., Кашия Ш.Р., Курмуков И.А.
Оптимальные сроки и режимы проведения
искусственного питания в интенсивной терапии //
Сonsilium medicumUkraina. – 2012. – Т. 6, № 7. –
С. 19-22.
- Пахомова Г.В., Подловченко Т.Г., Утешев Н.С.
Неотложная хирургия рака ободочной кишки // М.:
Миклош, 2009. – 95 с.
- Смирнова Г.О., Силуянов С.В. Периферическая
электрогастроэнтерография в клинической практике.
– Пособие для врачей / Под ред. Профессора В.А.
Ступина. – М.: «МЕДПРАКТИКА-М», 2009. – 20 с.
- Снеговой А.В., Салтанов А.И., Манзюк Л.В.,
Сельчук В.Ю. Нутритивная недостаточность и методы
ее лечения у онкологических больных //
Практическая онкология. – 2009. - Т. 10, № 1. – С.
49-57.
- Чиссов В.И., Старинский В.В., Петрова Г.В.
Злокачественные новообразования в России в 2008
году // М.: МНИОИ им. П.А. Герцена
Росмедтехнологий, 2010.- 256.
- Lassen K., Soop M., Nygren J. et.аl. 2009.
Consensus review of optimal perioperative care in
colorectal surgery: Enhanced Recovery After
Surgery (ERAS). Group recommendations Archives of
Surgery.– 144 (10) – 961-969.
Статья опубликована на сайте
http://www.gastroscan.ru
Если вы заметили орфографическую, стилистическую или другую ошибку на этой странице, просто выделите ошибку мышью и нажмите Ctrl+Enter. Выделенный текст будет немедленно отослан редактору
|
|
|
|

